
| A. | 某些花岗石产生氡(${\;}_{86}^{222}$Rn),从而对人体产生伤害,${\;}_{86}^{222}$Rn的质量数是222 | |
| B. | Se是人体必需的微量元素,${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se互为同位素,是两种不同的核素 | |
| C. | ${\;}_{92}^{235}$U的浓缩一直被国际社会关注,其中子数和质子数之差为51 | |
| D. | 113号元素属于过渡元素 |
分析 A.根据原子符号左上角的数字表示质量数分析;
B.质子数相同,中子数不同的同一元素的不同原子互称同位素,中子数=质量数-质子数,核素是指具有一定数目质子和一定数目中子的一种原子;
C.原子符号左上角的数字表示质量数,左下角的数字表示质子数,中子数=质量数-质子数;
D.过渡元素包括副族和ⅥⅡ族,111号元素处于13列.
解答 解:A.原子符号左上角的数字表示质量数,${\;}_{86}^{222}$Rn的质量数是222,故A正确;
B.${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se互质子数相同都为34,中子数分别为44、46,是两种不同的核素,故B正确;
C.${\;}_{92}^{235}$U的浓缩一直被国际社会关注,其质子数为92,中子数为235-92=143,两者之差为51,故C正确;
D.第七周期稀有气体原子序数=86+32=118,是第七周期最后一种元素,位于18列,113号元素处于第13列,故113号元素位于第七周期,ⅢA族,故D错误;
故选D.
点评 本题考查原子符号的意义、元素的推断,根据原子核外电子排布确定在周期表中的位置,熟练掌握核素的概念以及有关几“同”的概念,注意在原子中,核内质子数=核外电子数=核电荷数,质量数量=质子数+中子数是解答关键,题目难度不大.


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:选择题
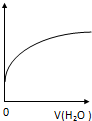
| A. | CH3COO-水解常数 | B. | 溶液中CH3COOH的数目 | ||
| C. | 溶液的PH | D. | 溶液中CH3COO- 的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中电子转移数为6 | B. | 生成的氯气式量约为73.3 | ||
| C. | KCl中既有35Cl,又有37Cl | D. | KCl中只含35Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S(s)+O2(g)═SO2(g)△H1;S(g)+O2(g)═SO2(g)△H2 | |
| B. | 2H2(g)+O2(g)═2H2O(g)△H1;2H2(g)+O2(g)═2H2O(l)△H2 | |
| C. | H2(g)+Cl2(g)═2HCl(g)△H1;$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H2 | |
| D. | CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H1;2CO(g)+O2(g)═2CO2(g)△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,D在元素周期表中的位置第3周期,第VIA族.
,D在元素周期表中的位置第3周期,第VIA族.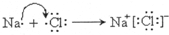 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原电池中电解质溶液能电离出自由移动的离子 | |
| B. | 有两根导线将两个活动性不同的电极连接 | |
| C. | 电极上进行的氧化还原反应的生成物为电子 | |
| D. | 电极上进行氧化还原反应时有电子的定向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO、NO能与人体的血红蛋白结合,使人中毒 | |
| B. | CaO能与SO2反应,可作工业废气的脱硫剂 | |
| C. | 光化学烟雾会引起呼吸道疾病 | |
| D. | CO2、NO2或SO2都会导致酸雨的形成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com