
(8��)��֪��Cu+2H2SO4(Ũ)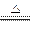 CuSO4+SO2��+2H2O����ͼ��ͭ��Ũ���ᷴӦ��ʵ��װ��ͼ����ش��������⡣
CuSO4+SO2��+2H2O����ͼ��ͭ��Ũ���ᷴӦ��ʵ��װ��ͼ����ش��������⡣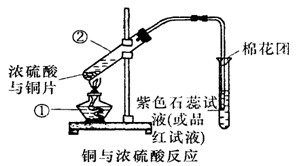
��1��д����Ţٵ����������ƣ� ������ ������
��2������������ͨ��Ʒ����Һ�е�����Ϊ�� �� ��
��3��ͼ�������н�������������Һ����������_________________________ ��������
��4����Ӧ������Ũ���ᱻ���ģ���ϡ����ͭ����ϡ���ᷴӦ����˷�Ӧ��ϣ��Թ���һ����������ʣ�ࡣ����ҩƷ��������֤����Ӧ���������Һ��ȷ���������________(����ĸ)��
a������ b��BaCl2��Һ c������ d��Na2CO3��Һ
 �γ̴����Ծ�����100��ϵ�д�
�γ̴����Ծ�����100��ϵ�д� �¾�����ĩ���100��ϵ�д�
�¾�����ĩ���100��ϵ�д� ȫ�ܴ���100��ϵ�д�
ȫ�ܴ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ��� | 5mlCuSO4��Һ | 10mlNaBr��Һ ��mol?L-1�� |
�� �� |
| �� | ��һ��CuSO4��Һ | a | ��Һ����ɫ��Ϊ����ɫ |
| �� | ��һ��CuSO4��Һ | b | ��Һ����ɫ��Ϊ����ɫ |
| �� | ��һ��CuSO4��Һ | c | ��Һ����ɫ��Ϊ����ɫ |
| ��� | 5mlCuSO4��Һ | 10mlNaBr��Һ ��mol?L-1�� |
�� �� |
| �� | d | ��һ��NaBr��Һ | ��Һ����ɫ��Ϊ����ɫ |
| �� | e | ��һ��NaBr��Һ | ��Һ����ɫ��Ϊ����ɫ |
| �� | f | ��һ��NaBr��Һ | ��Һ����ɫ��Ϊ����ɫ |
| ��� | 5mlCuSO4��Һ | 10mlNaBr��Һ ��mol?L-1�� |
�¶� | ���� |
| �� | ��һ��CuSO4��Һ | ��һ��NaBr��Һ | 25�� | ��Һ����ɫ��Ϊ����ɫ |
| �� | ��һ��CuSO4��Һ | ��һ��NaBr��Һ | 60�� | ��Һ����ɫ��Ϊ����ɫ |
| �� | ��һ��CuSO4��Һ | ��һ��NaBr��Һ | 75�� | ��Һ����ɫ��Ϊ����ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����



| ||
| �� |
| ||
| �� |
| ||
| �� |
| ||
| �� |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(8��)��֪��Cu+2H2SO4(Ũ)CuSO4+SO2��+2H2O����ͼ��ͭ��Ũ���ᷴӦ��ʵ��װ��ͼ����ش��������⡣
��1��д����Ţٵ����������ƣ� ������ ������
��2������������ͨ��Ʒ����Һ�е�����Ϊ�� �� ��
��3��ͼ�������н�������������Һ����������_________________________ ��������
��4����Ӧ������Ũ���ᱻ���ģ���ϡ����ͭ����ϡ���ᷴӦ����˷�Ӧ��ϣ��Թ���һ����������ʣ�ࡣ����ҩƷ��������֤����Ӧ���������Һ��ȷ���������________(����ĸ)��
a������ b��BaCl2��Һ c������ d��Na2CO3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010��ɳ��ҵˮƽ���Ը����ڶ���ģ�⻯ѧ���� ���ͣ�ʵ����
(8��)��֪��Cu+2H2SO4(Ũ)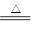 CuSO4+SO2��+2H2O����ͼ��ͭ��Ũ���ᷴӦ��ʵ��װ��ͼ����ش��������⡣
CuSO4+SO2��+2H2O����ͼ��ͭ��Ũ���ᷴӦ��ʵ��װ��ͼ����ش��������⡣
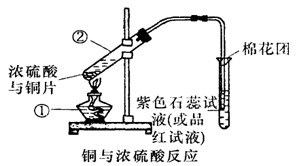
��1��д����Ţٵ����������ƣ� ������ ������
��2������������ͨ��Ʒ����Һ�е�����Ϊ�� �� ��
��3��ͼ�������н�������������Һ����������_________________________ ��������
��4����Ӧ������Ũ���ᱻ���ģ���ϡ����ͭ����ϡ���ᷴӦ����˷�Ӧ��ϣ��Թ���һ����������ʣ�ࡣ����ҩƷ��������֤����Ӧ���������Һ��ȷ���������________(����ĸ)��
a������ b��BaCl2��Һ c������ d��Na2CO3��Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com