
某研究性学习小组为测定某Na2CO3样品的纯度(其中只含NaHCO3杂质),选用下图所示的仪器装置进行实验(②装置未画全).试回答有关问题:
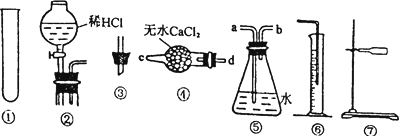
实验一:测定Na2CO3样品中NaHCO3分解放出CO2体积:连接装置的正确顺序是⑦①③④⑤⑥
(1)写出加热时发生反应的化学方程式________.
(2)完成该实验尚缺的仪器是________(填名称);产生气体从装置④的________进入,从装置⑤的________进入(填接口序号).
实验二:测定上述实验完成后剩余固体与盐酸反应产生CO2的体积.
(3)应将实验一的装置作哪些调整?________.
(4)当实验一加热至样品不再产生气体时,产生CO2体积为a L(已换算成标况下的体积,下同),则样品中NaHCO3的质量为________;实验二在加入盐酸至无气体产生时,生成CO2体积为b L,则Na2CO3样品的纯度为________.
误差分析:
(5)有同学建议将⑤中的水改用饱和的NaHCO3溶液,可以使测定结果更准确,请用平衡移动观点解释:________,同学为何没建议改用Na2CO3饱和溶液?请用离子方程式说明原因:________.
(6)有同学发现在实验一读取CO2体积时,⑥中液体的液面低于⑤中液体的液面,但未做任何处理,则a值________(填“偏大”、“偏小”或“无影响”).
科目:高中化学 来源: 题型:阅读理解
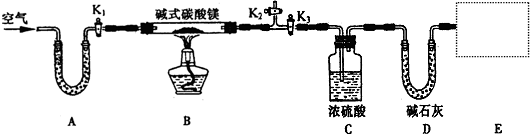
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
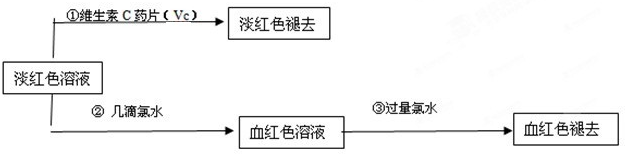
查看答案和解析>>
科目:高中化学 来源: 题型:
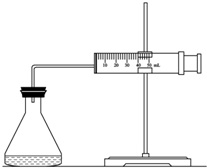 实验室用H2O2分解反应制取氧气时,常加入催化剂以加快反应速率,某研究性学习小组为研究催化剂FeCl3的量对O2生成速率的影响,设计了如下三组实验方案(见下表),将表中所给的试剂按一定体积混合后进行反应.
实验室用H2O2分解反应制取氧气时,常加入催化剂以加快反应速率,某研究性学习小组为研究催化剂FeCl3的量对O2生成速率的影响,设计了如下三组实验方案(见下表),将表中所给的试剂按一定体积混合后进行反应.| 实验编号 试剂 |
A | B | C |
| 10% H2O2/mL | 20.0 | V1 | V2 |
| 2mol/L FeCl3/mL | 0 | 5.0 | 10.0 |
| H2O/mL | V3 | V4 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
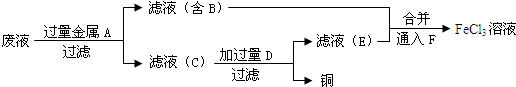
查看答案和解析>>
科目:高中化学 来源:2012-2013学年福建省5月高考三轮模拟化学试卷(解析版) 题型:填空题
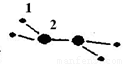
(1)M由两种短周期元素组成,每个M分子含有18个电子,其分子球棍模型如图所示。测得M的摩尔质量为32g/mol。画出编号为2的原子结构示意图: 。
(2)已知1.0mol·L—1NaHSO3溶液的pH为3.5,加入氯水,振荡后溶液pH迅速降低。溶液pH降低的原因是 (用离子方程式表示)。
(3)在常温常压和光照条件下,N2在催化剂(TiO2)表面与H2O反应,生成1molNH3和O2时的能量变化值为382.5kJ,达到平衡后此反应NH3生成量与温度的实验数据如下表。则该反应的热化学方程式为 。
|
T/K |
303 |
313 |
323 |
|
NH3生成量/(10—1mol) |
4.3 |
5.9 |
6.0 |
(4)在溶液中,一定浓度的NH4+能溶解部分Mg(OH)2固体,反应如下:
2NH4+(aq) + Mg(OH)2(s)
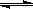 Mg2+(aq)
+2NH3·H2O(aq)
Mg2+(aq)
+2NH3·H2O(aq)
写出上述反应的平衡常数表达式
某研究性学习小组为探究Mg2+与NH3·H2O反应形成沉淀的情况,设计如下两组实验
|
实验① |
等体积1 mol/L氨水和0.1 mol/L MgCl2溶液混合 |
生成白色沉淀 |
|
实验② |
等体积0.1 mol/L氨水和1 mol/L MgCl2溶液混合 |
无现象 |
请分析实验①、②产生不同现象的原因: 。
(5)在室温下,化学反应I—(aq)+ ClO—(aq) = IO—(aq) + Cl—(aq)的反应物初始浓度、溶液中的氢氧根离子初始浓度及初始速率间的关系如下表所示:
|
实验编号 |
I—的初始浓度 (mol·L—1) |
ClO—的初始浓度 (mol·L—1) |
OH—的初始浓度 (mol·L—1) |
初始速率v (mol·L—1· s—1) |
|
1 |
2 × 10—3 |
1.5 × 10—3 |
1.00 |
1.8 × 10—4 |
|
2 |
a |
1.5 × 10—3 |
1.00 |
3.6 × 10—4 |
|
3 |
2 × 10—3 |
3 × 10—3 |
2.00 |
1.8 × 10—4 |
|
4 |
4 × 10—3 |
3 × 10—3 |
1.00 |
7.2 × 10—4 |
已知表中初始反应速率与有关离子浓度关系可以表示为v= k [I—]1 [ClO—]b [OH—]c(温度一定时,k为常数)。
①设计实验2和实验4的目的是 ;
②若实验编号4的其它浓度不变,仅将溶液的酸碱值变更为pH = 13,反应的初始速率v= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com