
【题目】在强酸性无色透明溶液中,下列各组离子能大量共存的是( )
A.Zn2+、Al3+、SO42-、Cl-B.Ag+、Na+、NO3-、Cl-
C.Fe3+、K+、Cl-、NO3-D.Ba2+、NH4+、Cl-、HCO3-
科目:高中化学 来源: 题型:
【题目】Ⅰ.现有x g某气体,它由三原子分子构成,它的摩尔质量为M gmol-1.若阿伏加德罗常数用NA表示,则:
(1)该气体所含原子总数为_____个。
(2)该气体在标准状况下的体积为______L。
(3)一个该气体分子的质量______g。
Ⅱ.(1)等物质的量的CO和CO2其原子数之比为 ______。
(2)同温、同压下,A、B两容器分别充满O2和O3 ,则O2和O3的密度之比为______,若两容器中O2和O3 所含原子总数相等,则A容器和B容器的容积比是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羟氡(NH2OH)为一元弱碱(25℃时,电离常数Kb=9.0×l0-9),其电离方程式为:NH2OH+H2O![]() NH3OH++OH-。用0.lmol/L盐酸滴定20mL0.lmol/L NH2OH溶液,恒定25℃时,滴定过程中由水电离出来的H+浓度的负对数与盐酸体积的关系如图所示(己知:lg3=0.5)。下列说法不正确的是( )
NH3OH++OH-。用0.lmol/L盐酸滴定20mL0.lmol/L NH2OH溶液,恒定25℃时,滴定过程中由水电离出来的H+浓度的负对数与盐酸体积的关系如图所示(己知:lg3=0.5)。下列说法不正确的是( )

A. A、B、C、D四点对应的溶液中NH2OH电离常数相等
B. A点对应溶液的pH=9.5
C. D点对应溶液中存在:c(H+)=c(OH-)+c(NH3OH+)+c(NH2OH)
D. C点时,溶液呈酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关除杂质(括号内物质为杂质)的方法中,错误的是
A. CH4(C2H4):酸性高锰酸钾溶液
B. NaHCO3溶液(少量Na2CO3):通入足量的CO2气体
C. 溴苯(混有Br2):加NaOH溶液洗涤、静置、分液
D. FeCl2溶液(FeCl3):加入过量铁,充分反应后过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则
(1)该反应的逆反应是________热反应,且m+n______(填“>”“<”或“=”)p。
(2)减压时,A的质量分数________(填“增大”“减小”或“不变”,下同)。
(3)若加入B(体积不变),则A的转化率________,B的转化率________。
(4)若升高温度,则平衡时,B、C的浓度之比![]() 将________。
将________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向体积均为10 mL、物质的量浓度相同的两份NaOH 溶液中分别通入一定量的CO2,得到溶液甲和乙。向甲、乙两溶液中分别滴加0.1mol/L的盐酸,此时反应生成CO2体积(标准状况)与所加盐酸体积的关系如图所示。则下列叙述中不正确的是
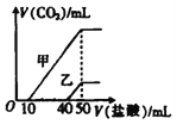
A. 原NaOH溶液的物质的量浓度为0.5 mol/L
B. 当0盐酸)<10 mL时,甲溶液中发生反应的离子方程式为H++CO32-=HCO3-
C. 乙溶液中含有的溶质是Na2CO3、NaOH
D. 向乙溶液中滴加过量盐酸后产生CO2体积的最大值为224 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列各组离子在指定溶液中一定能大量共存的是
A. 含有大量NO3-的溶液:H+、K+、Cl-、SO32-
B. 中性溶液:Fe3+、Al3+、NO3-、SO42-
C. ![]() 的溶液:K+、AlO2-、CO32-、Na+
的溶液:K+、AlO2-、CO32-、Na+
D. 由水电离出的c(H+) =10-12mol/L的溶液:Na+、K+、CO32-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. Fe2O3溶于氢碘酸:Fe2O3+6H+=2Fe3++3H2O
B. Na2SO3与稀硝酸:SO32-+2H+=SO2↑+H2O
C. AlCl3溶液中加入足量的氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
D. Ca(HCO3)2溶液中加入足量的氢氧化钠溶液:Ca2++2HCO3-+2OH-=CaCO3+CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】土壤中的硝酸盐会被细菌分解。有一种脱氮硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理如下:
5K2S+ 8KNO3 +4H2O![]() 4N2 ↑+5K2SO4 +8KOH
4N2 ↑+5K2SO4 +8KOH
还原剂是____________,还原产物是______________,
上述过程的发生改变了土壤的成分,从而对农业生产产生一定的不利影响,请选择任一角度进行简要说明:___________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com