
下列关于胶体的叙述不正确的是
A.布朗运动是胶体微粒特有的运动方式,可以据此把胶体和溶液.悬浊液区别开来
B.光线透过胶体时,胶体发生丁达尔现象
C.用渗析的方法净化胶体时,使用的半透膜只能让较小的分子.离子通过
D.胶体微粒具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳现象
 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源:2016-2017学年湖南省高二上期中化学卷(解析版) 题型:选择题
用0.2000 mol/L标准盐酸滴定待测烧碱的纯度,下列说法正确的是( )
A.滴定时可以用pH计或石蕊试液准确判断滴定终点
B.滴定前平视,滴定后俯视酸式滴定管,得出的滴定结果偏大
C.滴定前要用待测烧碱溶液洗涤锥形瓶
D.滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视锥形瓶内溶液颜色变化,直到滴定终点
查看答案和解析>>
科目:高中化学 来源:2017届广东省汕头市高三上期中化学试卷(解析版) 题型:选择题
高铁酸钾是一种高效绿色水处理剂,其工业制备的反应原理为:2Fe(OH)3 + 3KClO + 4KOH = 2K2FeO4 + 3KCl + 5H2O,下列说法正确的是
A.ClO ?做还原剂 B.Fe(OH)3在反应中被还原[
?做还原剂 B.Fe(OH)3在反应中被还原[
C .高铁酸钾中铁的化合价为+7 D.制备1molK2FeO4时转移3 mol 电子
.高铁酸钾中铁的化合价为+7 D.制备1molK2FeO4时转移3 mol 电子
查看答案和解析>>
科目:高中化学 来源:2017届广东省惠州市高三上学期调研一化学试卷(解析版) 题型:选择题
化学与生活、社会密切相关,下列有关说法中正确的是
A.“低碳生活”是指生活中尽量使用含碳量较低的物质
B.燃煤中加入CaO后可减少酸雨的发生及温室气体的排放
C.纤维素在人体内可水解为葡萄糖,是人类重要的营养物质之一
D.鼓励汽车、家电“以旧换新”,可减少环境污染,发展循环经济,促进节能减排
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一上期中考试化学试卷(解析版) 题型:选择题
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体(已知:NH4++OH-=NH3↑+H2O,Al(OH)3+OH-=AlO2-+2H2O),同时产生2.14g红褐色沉淀;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的白色沉淀。由此可知原溶液中
A.至少存在5种离子
B.Cl-一定存在,且c(Cl‑)≥0.4mol/L
C.SO42-、NH4+、Fe3+一定存在,Cl-可能不存在
D.CO32-、Al3+一定不存在,K+可能存在
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一上期中考试化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列说法中正确的是
A.0.1mol的NaHSO4溶液中含0.2NA个阳离子
B.1L0.1mol/L的乙醇溶液中所含的分子总数为0.1NA个
C.在标准状况下,含NA个氦原子(He)的氦气所含的分子数是0.5NA个
D.1molFeCl3跟沸水完全反应转化为氢氧化铁胶体,其中胶粒的数目一定少于NA个
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上期中化学试卷(解析版) 题型:填空题
将废旧锌锰电池处理得到含锰混合物,既能减少它对环境的污染,又能实现废电池的资源化利用。
Ⅰ. 回收二氯化锰:将废旧锌锰电池处理,得到含锰混合物,向该混合物加入浓盐酸并加热。
(1)写出MnO(OH)与浓盐酸反应的化学方程式:_________。
Ⅱ. 锰回收新方法:向含锰混合物加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止,其主要反应为:2MnOOH + MnO2 + 2H2C2O4 + 3H2SO4 == 3MnSO4 + 4CO2↑ + 6H2O
(2)与使用浓盐酸回收锰相比,新方法的优点是_________(答1点即可)。
(3)欲以MnSO4溶液为原料制备MnCO3,选用的加料方式___________(填字母),原因是___________。
已知:Ksp(MnCO3)=2.3×10﹣11、Ksp[Mn(OH)2]=2.1×10﹣13
a. 将MnSO4溶液与Na2CO3溶液同时加入到反应容器中
b. 将MnSO4溶液缓慢加入到盛有Na2CO3溶液的反应容器中
c. 将Na2CO3溶液缓慢加入到盛有MnSO4溶液的反应容器中
d. 以上三种方式都无法得到MnCO3.
Ⅲ. 现以含锰混合物为原料制备锰锌铁氧体的主要流程如图l所示:
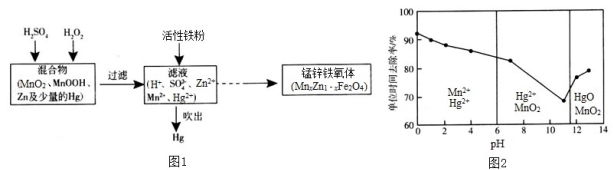
请回答下列问题:
(4)MnxZn1﹣xFe2O4中铁元素化合价为+3,则锰元素的化合价为___________。
(5)活性铁粉除汞时,铁粉的作用是_________(填“氧化剂”或“还原剂”)。
(6)酸浸时,MnO2与H2SO4、H2O2反应的离子方程式为__________________。
(7)除汞是以氮气为载气吹入滤液中,带出汞蒸气经KMnO4溶液进行吸收而实现的。在恒温下不同pH时,KMnO4溶液对Hg的单位时间去除率及主要产物如图2所示:
①写出pH=10时KMnO4溶液吸收汞蒸气的离子方程式________________。
②在强酸性环境中汞的单位时间去除率高,其原因除氢离子浓度增大使KMnO4溶液的氧化性增强外,还可能是__________________。
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三11月模拟化学卷(解析版) 题型:选择题
香叶醇是合成玫瑰香油的主要原料,其结构简式如图。下列有关香叶醇的叙述正确的是( )
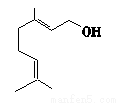
A.香叶醇的分子式为C10H18O
B.不能使溴的四氯化碳溶液褪色
C.不能使酸性高锰酸钾溶液褪色
D.能发生加成反应不能发生取代反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江双鸭山一中高一上期中考试化学试卷(解析版) 题型:选择题
12mL浓度为0.10mol?L-1的Na2SO3溶液,恰好与10mL浓度为0.04mol?L-1的K2Cr2O7溶液完全反应,已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则元素C r在还原产物中的化合价为
r在还原产物中的化合价为
A.+5
B.+4
C.+3
D.+2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com