
【题目】有关下列图象的分析错误的是( )
A. 图可表示对平衡N2(g)+3H2(g)2NH3(g)加压、同时移除部分NH3时的速率变化
图可表示对平衡N2(g)+3H2(g)2NH3(g)加压、同时移除部分NH3时的速率变化
B.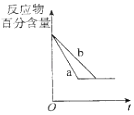 图中a、b曲线只可表示反应H2(g)十I2(g)2HI(g)在有催化剂和无催化剂存在下建立平衡的过程
图中a、b曲线只可表示反应H2(g)十I2(g)2HI(g)在有催化剂和无催化剂存在下建立平衡的过程
C. 图表示向CH3COOH溶液中逐渐加入CH3COONa固体后,溶液pH的变化
图表示向CH3COOH溶液中逐渐加入CH3COONa固体后,溶液pH的变化
D. 图表示向醋酸溶液中加水时其导电性变化,则CH3COOH溶液的pH:a<b
图表示向醋酸溶液中加水时其导电性变化,则CH3COOH溶液的pH:a<b
【答案】BC
【解析】解:A、图可表示对平衡N2(g)+3H2(g)2NH3(g)加压、同时移除部分NH3时的速率变化,所以瞬间正反应速率加快,逆反应速率减慢,所以平衡正向移动,故A正确; B、两边气体的计量数相等,还可以是压强的变化,不一定是催化剂的影响,故B错误;
C、加入CH3COONa固体,对醋酸的电离起抑制作用,溶液的PH值变大,而不是减小,故C错误;
D、导性越强自由移动离子的浓度越大,所以a点氢离子的浓度大于b点,所以CH3COOH溶液的pH:a<b,故D正确;
故选BC.
A、图可表示对平衡N2(g)+3H2(g)2NH3(g)加压、同时移除部分NH3时的速率变化,所以瞬间正反应速率加快,逆反应速率减慢;
B、两边气体的计量数相等,还可以是压强的变化;
C、加入CH3COONa固体,对醋酸的电离起抑制作用;
D、导性越强自由移动离子的浓度越大.


科目:高中化学 来源: 题型:
【题目】中学化学中的一些常见物质有如图转化关系(部分产物未给出).其中A、H的焰色呈黄色,D常温下为黄绿色气体,反应③为侯氏制碱法反应原理之一,E是常见的金属.
回答下列问题.
(1)D的电子式为 .
(2)H的化学式为 .
(3)写出反应①的化学方程式 .
(4)写出反应②的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)原子、元素、核素、同位素等都属于重要的化学基本概念。下列八种化学符号: ![]()
①涉及到的元素有______种,核素共有______种;
②互为同位素的是__________,____________;
(2)在H、O、C、Na四种元素中,选择适当的元素组成符合下列要求的物质,将它们的化学式填写在以下空格中。(注意:每种物质只能出现一次)
酸性氧化物 | 碱性氧化物 | 酸 | 碱 | 电解质 | 非电解质 |
_______ | _______ | ______ | ______ | _______ | _______ |
(3)下列各组物质的分离或提纯,应选用下述方法的哪一种?(填选项字母)
A.分液 B.过滤 C.萃取 D.蒸馏 E.蒸发结晶 F.高温分解
①分离CCl4和H2O:______;
②除去澄清石灰水中悬浮的CaCO3:______;
③除去CaO固体中少量的CaCO3固体:______;
④从碘水中提取碘:______;
⑤分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为V L的恒容密闭容器中盛有一定量H2 , 通入Br2(g)发生反应H2(g)+Br2(g)2HBr(g)△H<0.当温度分别为T1、T2 , 平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法正确的是( ) 
A.若b、c两点的平衡常数分别为K1、K2 , 则K1>K2
B.a、b两点的反应速率:b>a
C.为了提高Br2(g)的转化率可采取增加Br2(g)通入量的方法
D.b、c两点的HBr的体积分数b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用质量分数为98℅、密度为1.84g/mL的浓硫酸来配制480mL 0.2mol/L 的稀硫酸。可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥容量瓶 ⑦托盘天平 ⑧药匙。完成下列问题:
(1)上述仪器中,在配制稀硫酸时不需要用到的是___________(填序号)
(2)配制过程中需选用的容量瓶规格为___________ mL,经过计算,需要浓硫酸的体积为_______。
(3)在配制过程中,下列操作错误的是____________,能使所配溶液浓度偏高的是___________(填序号)
①洗涤量取浓硫酸后的量筒,并将洗涤液转移至容量瓶中
②为防止变质,稀释后的硫酸溶液应立即就转移到容量瓶中
③将浓硫酸直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓硫酸
④移液前,容量瓶中含有少量蒸馏水
⑤量取浓硫酸时,俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)①Cu ②CO2 ③H2SO3④H2O⑤液态HCl ⑥H2SO4⑦Ba(OH)2 ⑧NaCl ⑨蔗糖 ⑩NaOH溶液
上述物质中属于电解质的是______________,属于非电解质的是________,能导电的是_________。 (填序号,必须填全,否则不得分)
(2)与16g氧气所含原子总数相同的氨气是_________________g。
(3)已知实验室制取氯气的反应原理为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
①该反应中氧化剂和还原剂的物质的量之比为________
②当2 mol MnO2参加反应时转移电子______mol
③当转移1 mol电子时能生成标准状况下的Cl2______L
④浓盐酸在反应中显示出来的性质是______(填字母)
a.还原性 b.酸性 c.氧化性 d. 挥发性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列各题。
(1)向澄清石灰水中通入过量CO2(写出离子方程式)___________________________________
(2)用稀硫酸洗铁锈(Fe2O3)(写出离子方程式)____________________________________
(3)2Al + 6H+ = 2Al3+ + 3H2↑(写出对应的化学方程式并用双线桥法标出电子转移情况)__________________
(4)在一定条件下,某化合物W受热分解:2W ![]() A↑+2B↑+4C↑,测得反应后生成的混合气体的密度是相同条件下H2密度的12倍,则W的摩尔质量是 _______
A↑+2B↑+4C↑,测得反应后生成的混合气体的密度是相同条件下H2密度的12倍,则W的摩尔质量是 _______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能获得成功的是
A. 苯与浓溴水用铁作催化剂制溴苯B. 可用分液漏斗分离硝基苯和水
C. 将苯与浓硝酸混合共热制硝基苯D. 加入水后分液可除去溴苯中的溴
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com