

| A. | BaCl2、H2SO4、MgCl2 | B. | CaCl2、HNO3、BaCl2 | ||
| C. | CaCl2、HNO3、NaCl | D. | BaCl2、HCl、Na2SO4 |
分析 可以和碳酸钠生成的白色沉淀可以是碳酸钡、碳酸钙,该沉淀能溶于强酸中,得到含有钙离子或是钡离子以及酸根阴离子的盐,根据复分解反应的条件,加入的丙中可以含有硫酸根离子或是其他离子的化合物,根据物质的性质以及物质间反应的实验现象进行分析解答即可.
解答 解:可以和碳酸钠生成的白色沉淀可以是碳酸钡、碳酸钙,该沉淀能溶于强酸中,得到含有钙离子或是钡离子以及酸根阴离子的盐,根据复分解反应的条件,加入的丙中可以含有硫酸根离子或是其他离子的化合物.
A、碳酸钠能与氯化钙反应生成碳酸钡沉淀,碳酸钡中加入硫酸,则硫酸与碳酸钡反应生成硫酸钡沉淀,沉淀不会消失,故A错误;
B、碳酸钠能与氯化钙反应生成碳酸钙沉淀,加入硝酸,则沉淀完全溶解并产生气体,加入BaCl2不会产生白色沉淀,故B错误;
C、碳酸钠能与氯化钙反应生成碳酸钙沉淀,加入硝酸,则沉淀完全溶解并产生气体,加入氯化钠不会产生白色沉淀,故C错误;
D、碳酸钠能与氯化钙反应生成碳酸钡沉淀,碳酸钡中加入盐酸,则沉淀完全溶解并产生气体,加入硫酸钠,会反应,得到硫酸钡沉淀,故D正确;
故选D.
点评 掌握物质的性质以及物质间反应的实验现象是正确解答本题的关键,难度中等.


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案科目:高中化学 来源: 题型:多选题
| A. | 用锌粒代替锌粉 | B. | 向其中加入少量1mol/L硫酸溶液 | ||
| C. | 向其中加入氯化钠溶液 | D. | 向其中加入等体积的水 | ||
| E. | 向其中加入碳酸钠溶液 | F. | 向其中加入硝酸钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的NaHCO3和Na2CO3与足量盐酸反应,在相同条件下NaHCO3产生的CO2体积大 | |
| B. | 等物质的量的两种盐与同浓度盐酸完全反应,所消耗盐酸的体积Na2CO3是NaHCO3的两倍 | |
| C. | 将石灰水加入NaHCO3溶液中无沉淀,加入Na2CO3溶液中有白色沉淀 | |
| D. | 等浓度的两种盐溶液分别与等浓度的盐酸反应,碳酸氢钠溶液的反应速率快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲酸乙酯 | B. | 乙酸甲酯 | C. | 乙酸丙酯 | D. | 丙酸丁酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
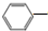 CH2CH3(g)+Cl2(g)$\stackrel{催化剂}{?}$
CH2CH3(g)+Cl2(g)$\stackrel{催化剂}{?}$ CHCl-CH3(g)+HCl(g)△H>0
CHCl-CH3(g)+HCl(g)△H>0| 时间/(min) | 0 | 2 | 5 | 6 | 9 | 10 |
| χ(乙苯) | 0.5 | 0.25 | 0.1 | 0.1 | 0.05 | 0.05 |
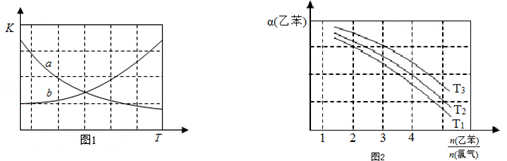
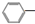 CH2CH3(g)$\stackrel{催化剂}{?}$
CH2CH3(g)$\stackrel{催化剂}{?}$ CH=CH2(g)+H2(g)△H=+124kJ/mol
CH=CH2(g)+H2(g)△H=+124kJ/mol查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com