
����Ŀ��ijһԪ����(��HA��ʾ)��ˮ�еĵ��뷽��ʽ�ǣ�HA![]() H����A�����ش��������⣺
H����A�����ش��������⣺
��1������Һ�м�������NaA���壬����ƽ�⽫��________(����������������)��Ӧ�����ƶ���������________ ��
��2��������Һ�м�������NaCl��Һ������ƽ�⽫��______(����������������)��Ӧ�����ƶ�����Һ��c(A��)��________(����������������С������������)����Һ��c(OH��)��________(����������������С������������)��
��3����25 ���£���a mol��L��1�İ�ˮ��0.01 mol��L��1������������ϣ���Ӧƽ��ʱ��Һ��c(NH4+)��c(Cl-)������Һ��_______��(������������������������)���ú�a�Ĵ���ʽ��ʾNH3��H2O�ĵ��볣��Kb��______ ��
���𰸡��� c(A��)����ƽ�����Сc(A��)�ķ����淴Ӧ�����ƶ� �� ��С ���� �� 10��9/(a��0.01) mol��L��1
��������
��1��ijһԪ����(��HA��ʾ)��ˮ�еĵ��뷽��ʽ�ǣ�HA![]() H����A����������Һ�м�������NaA����ʱ�����ܽ�������A����ʹ��Һ��c(A��)������ƽ���ƶ�ԭ���������������Ũ�ȣ�ƽ��������A-���ӵķ����ƶ���ʹc(A��)��С�����ƽ�������ƶ���HA����̶ȼ�С��
H����A����������Һ�м�������NaA����ʱ�����ܽ�������A����ʹ��Һ��c(A��)������ƽ���ƶ�ԭ���������������Ũ�ȣ�ƽ��������A-���ӵķ����ƶ���ʹc(A��)��С�����ƽ�������ƶ���HA����̶ȼ�С��
(2)������Һ�м�������NaCl��Һ��NaCl���������Na+��Cl-��ƽ���ƶ��أ�������Һ�е�ˮ����Һ��ϡ�����ã�ʱ����ʷ��ӡ����ӵ�Ũ�ȶ���С���������ӵ�ϵ��������ϡ�͵ı��������Ը���ƽ���ƶ�ԭ����֪�����ϵ���ƽ�⽫������Ӧ�����ƶ�������ϡ������ʹ����Ũ�ȼ�С�����ƴ���ƽ�������ƶ�ʹ����Ũ����������ƣ�������Һ��c(A��)����С����Һ��c(H+)Ҳ��С����������Һ�д���ˮ�ĵ���ƽ�⣬ˮ�����ӻ��Ǹ�������Kw= c(H+)��c(OH��)=������c(H+)��С������c(OH��)������
(3)���κ���Һ�ж����ڵ���غ㣬��25 ���£���a mol��L��1�İ�ˮ��0.01 mol��L��1������������ϣ������Һ�У�c(NH4+)+ c(H+)��c(Cl-)+ c(OH��)�����ڷ�Ӧƽ��ʱ��Һ��c(NH4+)��c(Cl-)����c(H+)= c(OH��)��������Һ���У��ú�a�Ĵ���ʽ��ʾNH3��H2O�ĵ��볣��Kb��![]()


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Cl2���仯�����������������о��й㷺����;������������ˮ���γ���������ˮ��ϵ��
���������գ�
��1����ԭ���������ӵĵ����Ų�ʽ��__��������Ų�ʽ��ȣ������ʾʽ�����˶Ժ�������˶�״̬��__������
��2���⡢�ȡ�������Ԫ�ظ����γ�һ�ּ������ӣ������Ӱ뾶�ɴ�С��˳��������Щ����__��
��3����������ˮ��ϵ�У����ڶ������Ԫ�ص�ƽ���ϵ����ֱ���ƽ�ⷽ��ʽ��ʾ��__����֪HClO��ɱ��������ClO��ǿ���ȴ�������ˮʱ�����ļ���ɱ��Ч�����ڶ��������ԭ����__��һ��ԭ�ɣ���
��4������ˮ�У����й�ϵ��ȷ����__��ѡ���ţ���
a c��HClO��+c��ClO����=c��H+����c��OH����
b c��H+��=c��ClO����+c��Cl����+c��OH����
c c��HClO����c��Cl����
d c��Cl������c��OH����
��5��ClO2��һ�ָ���Ч����ȫ������������ҵ�Ͽ���ClO2��ˮ�е�MnCl2�ڳ����·�Ӧ������MnO2�����ᣬ�Գ�ȥˮ��Mn2+��д���÷�Ӧ�Ļ�ѧ����ʽ������ƽ��__��������Ϊ����MnO2������������Ӧ����������������ʶ����__����������������������˵������__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС����ȡ����غ���ˮ�������й�̽��ʵ�顣
ʵ��һ ��ȡ����غ���ˮ
������ͼ��ʾ��ʵ��װ�ý���ʵ�顣

��1����ȡʵ�������ȡ��B���Թ���ȴ�ᾧ�����ˣ�ϴ�ӡ���ʵ�����������Ҫ�IJ���������______��
��2�����Ե�B��Cװ�õ�λ�ã�_____�����������������������������B������صIJ��ʡ�
ʵ��� �������⻯�ط�Ӧ���о�
��3���ڲ�ͬ������KClO3�ɽ�KI����ΪI2��KIO3����С�������ϵ��ʵ���о���Ӧ�����Է�Ӧ�����Ӱ�죬����ϵ��aʵ��ļ�¼�����£�ʵ���������½��У���
�Թܱ�� | 1 | 2 | 3 | 4 |
0.20molL-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3��s��/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0molL-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
����ˮ/mL | 9.0 | 6.0 | 3.0 | 0 |
ʵ������ |
��ϵ��aʵ���ʵ��Ŀ����______��
�����1���Թ�ʵ���������______��
����2���Թ�ʵ����������Һ��Ϊ��ɫ��ȡ��������Һ����______��Һ����ɫ��
ʵ���� �ⶨ������ˮ����Ԫ�ص�����
��4�������������ϣ�Ϊ��С�����һ�����е�ʵ�鷽�������������������̵�ϸ�ڣ���_____��
���ϣ��ٴ�������ƻ����ָʾ����
�ڴ��������ˮ�ɱ�SO2��H2O2��FeCl2�����ʻ�ԭ��Cl-��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҵ����׳ƾƾ����������������ᡢ���ϡ��㾫��Ⱦ�ϡ�ȼ�ϵȡ�
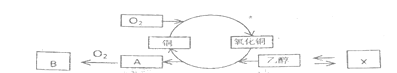
��1����д���ṹ��ʽA��___��B��___��
��2��ͼʾ�������Ҵ�ת��ΪA���÷�Ӧ����Ϊ��___�������Ҵ�������___��Ӧ(��������"������ԭ��)���Ҷ���(HO-CH2-CH2-OH)Ҳ�ܷ������Ʒ�Ӧ����д����Ӧ����ʽ��___��
��3������д��X�Ļ�ѧʽ___��������ط�Ӧ����ʽ֤ʵX�����Ҵ��ת��___��
��4����ҵ�ϳ���ƻ���ƻ������Ѿƻ�����ѿ����������������������ᣬ���Ǵ���ɫ��ѧ�Ƕȣ��÷����ڲ��㣬��д��һ������֮����___���������ֱ���ù�ҵ�ƾ����÷�ԭ�����Ʒ���������������á�
��5���������Ҵ���һ�������¿ɷ�Ӧ��������������������-18ͬλ��ʾ�ٷ�д���÷�Ӧ�Ļ�ѧ����ʽ��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ж���ȷ���� �� ��
A.��ϡ��ˮ�м�ˮϡ�ͣ�![]() ������
������
B.������HA>HB��������ʵ���Ũ�ȵ������NaA��NaB��Һ����й�ϵ�� c(OH-)>c(A-)>c(B-)>c(H+)
C.0.1 mol��L-1��һ����ҺpH�ɴ�С����Ϊ�� NaOH>Na2CO3>NaHSO4>��NH4��2SO4
D.�ֱ�ϡ��10mLpH=1������ʹ�����100mL������pH�仯��˵������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��KMnO4��һ�ָ�Ч���������������������л���ζ��.Ҳ������ˮ�е���������������̡����衢�ӵȷ�Ӧ��ʵ���ҳ���Na2C2O4����Һ�궨δ֪Ũ�ȵ�KMnO4��Һ��������Ӧ:5C2O42-+2MnO4-+16H++4H2O=2[Mn(H2O)6]2++10CO2��������������Ϣ,�����������:
(1)�������Ų�Kλ��Ԫ�����ڱ���_______��,��̬Mn2+�ĺ�������Ų�ʽ�ɱ�ʾΪ_____��
(2)1 mol [Mn( H2O)6]2+�������еĹ��ۼ���ĿΪ__________��
(3)��̬Cԭ�ӵĺ��������ռ������ܼ��ĵ���������ͼΪ_______.C2O42-��̼ԭ�ӵĹ���ӻ�������___________________.
(4)ͬ����Ԫ������������Ӧ����⻯��ķе�:H2O>H2Se>H2S,ԭ����__________��
(5)��-MnSe�Ľṹ��SeΪ�����������ܶѻ��������ṹ��ͼ��ʾ��
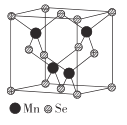
����-MnSe��Mn����λ��Ϊ_____________��
�����þ���ľ�������Ϊapm,�����ӵ�������ֵΪNA������������������ԭ��֮��ľ���Ϊ______pm, ��-MnSe ���ܶ���= ______ ( �г�����ʽ)g��cm-3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪![]() �����ԭ������Ϊ34.969���������˵����ȷ����( )
�����ԭ������Ϊ34.969���������˵����ȷ����( )
A.��Ԫ�صĽ������ԭ������Ϊ35
B.��Ԫ�ص�ij��ͬλ�ص�������Ϊ35
C.��Ԫ�ص�������Ϊ18
D.��ԭ�ӵ�����Ϊ34.969
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ������ܵı�����ȷ����( )
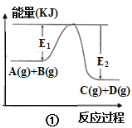

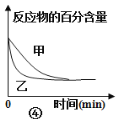
A.ͼ�ٱ�ʾ��ӦA(g)��B(g)��C(g)��D(g)�����ȷ�Ӧ����������(E2-E1)kJ
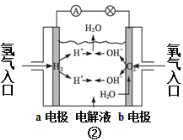
B.ͼ��Ϊ����ȼ�ϵ��ʾ��ͼ����������ͨ����������֮��Ϊ2��1
C.ͼ��������a��b���ܽ�����ߣ��������ؽᾧ����a��b��������ᴿa
D.ͼ�ܿɱ�ʾѹǿ�Է�Ӧ2A(g)��B(g)![]() 3C(g)��D(s)��Ӱ�죬���ҵ�ѹǿ��
3C(g)��D(s)��Ӱ�죬���ҵ�ѹǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�ֳ���ˮ����������ʳ���������Ѹɣ�����֮�⣬���ѻ���������ơ�
(1)��������֭���������ǵķ����ǣ������мӼ�������ԣ��ټ������Ƶ�Cu(OH)2�����ȣ���������________��
(2)��������ƹ����У�������ת��Ϊ�ƾ��Ĺ������£�����������л�ѧ����ʽ��C6H12O6(������)![]() 2_________+ 2 C2H5OH
2_________+ 2 C2H5OH
(3)���Ѿ��ܷⴢ������л���������ζ�����࣬����Ҳ����ͨ����ѧʵ�����Ʊ���ʵ���ҿ�����ͼ��ʾװ���Ʊ�����������

���Թ�a���������������Ļ�ѧ����ʽ��__________��
���Թ�b��ʢ�ŵ��Լ��DZ���____________��Һ��
��ʵ�鿪ʼʱ���Թ�b�еĵ��ܲ�����Һ���µ�ԭ����________��
����Ҫ������Թ�b�е�������������Ҫ�õ���������_______(����ĸ)��
A.��ͨ©�� B.��Һ©�� C.����©��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com