
����Ŀ���úڱ���(��Ҫ�ɷ�ΪBaS)�����̿�(��Ҫ�ɷ�ΪMnO2)Ϊԭ����ȡBa(OH)2��8H2O��MnCO3�Ĺ����������£�
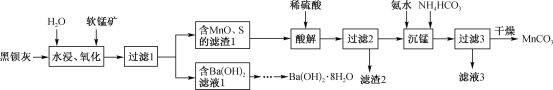
�ش��������⣺
(l)��ˮ����������ʱ��BaS��ת��ΪBa(OH)HS��Һ��MnO2������Ba(OH)HS��д���ڶ�����Ӧ�Ļ�ѧ����ʽ��_________________________��
(2)����1������Ba(OH)2��Һ���Ƶ�Ba(OH)2��8H2O�����辭���ľ���ʵ�������_________��������õ�Ba(OH)2��8H2O��Ʒ[��֪Ba(OH)2��20�桢60�桢80��ʱ�ܽ������Ϊ:3.76g��17.65g��101.4g]��
(3)������2������Ҫ�ɷ�Ϊ_______(�ѧʽ)����������ʱ������Ӧ�����ӷ���ʽΪ________������Һ3���пɻ��յIJ�ƷΪ__________(�ѧʽ)��
���𰸡�MnO2+Ba(OH)HS=MnO+S+ Ba(OH)2 ����Ũ������ȴ�ᾧ�����ˡ�ϴ�� S Mn2++ NH3��H2O+HCO3-=MnCO3��+NH4++H2O (NH4)2SO4
��������
(l)��ˮ����������ʱ��BaS��ת��ΪBa(OH)HS��Һ��MnO2������Ba(OH)HS��������ͼ��֪����Ӧ����ΪMnO��S�ȣ��ɴ˿�д���ڶ�����Ӧ�Ļ�ѧ����ʽ��
(2)����1������Ba(OH)2��Һ���Ƶ�Ba(OH)2��8H2O�����辭������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ�������õ�Ba(OH)2��8H2O��
(3)��ϡ�����ܽ�MnO��S ��MnO��ϡ���ᷴӦ����S����Ӧ���ɴ˱��ȷ��������2������Ҫ�ɷ֣���������ʱ�������백ˮ��̼����立�Ӧ������MnCO3������淋ȣ�Ҳ�͵ó�����Һ3���пɻ��յIJ�Ʒ��
(l)������ͼ��֪��MnO2����Ba(OH)HS������MnO��S�ȣ���Ӧ�Ļ�ѧ����ʽΪMnO2+Ba(OH)HS=MnO+S+ Ba(OH)2����Ϊ��MnO2+Ba(OH)HS=MnO+S+ Ba(OH)2��
(2)����Ba(OH)2��Һ���Ƶ�Ba(OH)2��8H2O��������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ�������õ�Ba(OH)2��8H2O����Ϊ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ�
(3)��ϡ�����ܽ�MnO��S��MnO+H2SO4=MnSO4+H2O����S����Ӧ����������2������Ҫ�ɷ�ΪS����������ʱ��������Ӧ�Ļ�ѧ����ʽΪMnSO4+ NH3��H2O+NH4HCO3=MnCO3��+(NH4)2SO4+H2O�����ӷ���ʽΪMn2++ NH3��H2O+HCO3-=MnCO3��+NH4++H2O������Һ3���пɻ��յIJ�ƷΪ(NH4)2SO4����Ϊ��S��Mn2++ NH3��H2O+HCO3-=MnCO3��+NH4++H2O��(NH4)2SO4��


 ���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д�
���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д� ���Ͱ�ͨ������ϵ�д�
���Ͱ�ͨ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾÿһ�����ʾһ�ַ�Ӧ������������A��C��D��E��F��ͨ������¾�Ϊ���壬�Ҽ���X���ɵ�A��C�����ʵ���֮��Ϊ1��1��BΪ����Һ�塣
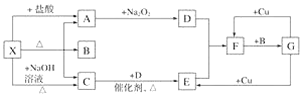
�Իش��������⣺
(1)X��________(�ѧʽ����ͬ)��F��__________��
(2)A�D��D��Ӧ�Ļ�ѧ����ʽΪ_______��
(3)G��Cu�ķ�Ӧ�У�G���ֵ�����Ϊ______��
(4)X�����NaOH��Һ��Ӧ����C�����ӷ���ʽΪ_____________��
(5)��C��B��DΪԭ�Ͽ�����G����ʹamol C��ȫת��ΪG��������������ҪD___ mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ѧ��ѧ�г����ڻ����ķ�����ᴿ��װ�ã������װ�ûش����⣺
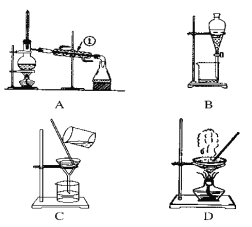
(1)���Ȼ�����Һ�еõ��Ȼ��ع��壬ѡ��װ��________(�����װ��ͼ����ĸ����ͬ)����ȥ����ˮ�е�Cl�������ʣ�ѡ��װ��________��
(2)�ӵ�ˮ�з����I2��ѡ��װ��________���÷��뷽��������Ϊ________��
(3)װ��A�Тٵ�������________����ˮ�ķ����Ǵ�________�ڽ�ˮ��װ��B�ڷ�ҺʱΪʹҺ��˳�����£��������⣬��Ӧ���еľ��������____��
(4)��ˮ���̲��ŷḻ����Դ����ʵ������ȡ������ˮ�������������̵�ʵ�飺
![]()
![]()
![]()
![]()
![]() �D��
�D��![]()
�����к�Ca2����Mg2����Fe3����SO42-�����ʣ���Ҫ�ᴿ������ۺ����á������ᴿ�IJ����У�
�ټ��������Na2CO3��Һ���ڼ��������BaCl2��Һ���ۼ��������NaOH��Һ���ܵ�����Һ��pH����7�����ܽ⡡���ˡ�������
��ȷ�IJ���˳����________(��ѡ����ĸ)��
a���ݢڢۢ٢ޢܢ� b���ݢ٢ڢۢޢܢ�
c���ݢڢ٢ۢܢޢ� d���ݢۢڢ٢ޢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ�������ɣ��ж�������䣬������ȷ������ǣ� ��
�ټ�������ʵ��۵���ԭ�����������������
����(![]() )�ǵڢ�
)�ǵڢ�![]() �壬���⻯����ȶ���С��
�壬���⻯����ȶ���С��![]()
�۸���ͬ����Ԫ�صĵ�һ�����ܱ仯���ƣ��Ƴ�Al�ĵ�һ�����ܱ�Mg��
�ܵڶ����ڷǽ���Ԫ�ص���̬�⻯������ˮ��ˮ��Һ��Ϊ����
����(![]() )����ͬ���壬�䵥�ʼ��������ᷴӦ������������������Һ��Ӧ
)����ͬ���壬�䵥�ʼ��������ᷴӦ������������������Һ��Ӧ
����X+��Y2���ĺ�����Ӳ�ṹ��ͬ����ԭ��������X>Y
A.�٢ۢ�B.�٢ڢ�C.�ۢܢ�D.�ڢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȼ���д��ڴ����Ľ���Ԫ�أ������ơ�þ����������ͭ���ڹ�ũҵ���������Ź㷺��Ӧ�á��ش���������:
(1)CuSO4��Cu(NO3)2�������Ӻ�������Ų�ʽΪ__________��N��O��SԪ�ص�ԭ�ӶԼ��ϵ���������������___________��
(2)������ͭ��Һ�м������KCN������������[Cu(CN)4]2-��1mol CN�к��е���������ĿΪ__________����CN��Ϊ�ȵ���������ӻ������__________(д��һ�ּ���)��
(3)[Cu(NH3)4]2+�У��ṩ�¶Ե��ӵ���___________��Cu(NH3)2Cl2������ͬ���칹�壬����һ�ֿ�����ˮ������ֻ�������___________(���������������Ǽ�����)���ӣ��ɴ���֪[Cu(NH)4]2+�Ŀռ乹����___________��������ƽ��������������������������
(4)NH3��Nԭ�ӵ��ӻ���ʽ��___________����Ԫ�ض�Ӧ�ĺ�����������H2SO4ǿ��H2SO3����ԭ��Ϊ___________��
(5)ͭ��һ�������ᄃ��ṹ��ͼ��ʾ����������Ļ�ѧʽ��___________�����þ���ṹΪ�����壬�������ͼ�������ӵ�����ΪNA�������������ܶ�Ϊ___________g/cm3��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(AlN)��һ�ֻҰ�ɫ���壬����ˮ������Ӧ������NH3��Al��800�����Ϸ�Ӧ���Ʊ�AlN��ʵ��װ�����£�
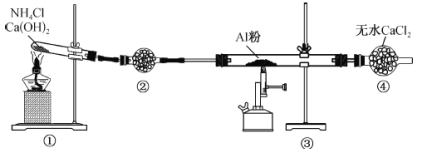
�ش��������⣺
(1)װ�â���ʢ�ŵ�ҩƷΪ__________��װ�âܵ����������հ�����__________��
(2)ʵ��ʱ�ȵ�ȼ�ٴ��ƾ��ƣ���Ŀ����______________________________________��
(3)Ϊʹʵ�鰲ȫ��װ�âܵ�β������������_____________________��
(4)װ�â��з�����Ӧ�Ļ�ѧ����ʽΪ_____________________��װ�â��з�����Ӧ�Ļ�ѧ����ʽΪ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��.FeCl3����ѧʵ���ҳ��õ��Լ������������Ʊ������������塣
�����Ʊ�������������IJ���������ȷ����____________������ĸ����
A�����Ȼ�����Һ�еμ���������������ϡ��Һ
B����������Ȼ���������Һ
C���ڰ�ˮ�еμ��Ȼ���Ũ��Һ
D���ڷ�ˮ�еμӱ����Ȼ�����Һ�������Һ��ʺ��ɫ��
��2��д��Ba(OH)2��Һ������NaHCO3��Һ��Ӧ�����ӷ���ʽ:___________________��
��3��д��������ĵ���ʽ��________________��д�����������д��ڵ����л�ѧ�����ͣ�____________________��
��4�������к������ۣ��ɼ�______��ȥ���ʣ������Ļ�ѧ����ʽΪ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ѱ�(TiO2)����Ҫ�İ�ɫ������LiFePO4������ӵ�ص��������ϡ�һ������������( ��Ҫ�ɷ�ΪFeTiO3 ������Fe2O3 )�����Ѱۺ�LiFePO4 ������������������ͼ��ʾ:

�ش���������:
��1�� LiFePO4��Fe�Ļ��ϼ���_______________________��
��2����������������ǰ��Ҫ���з����������Ŀ����__________________________________��
��3�������ӷ���ʽ��ʾ����I�������۵�Ŀ��:__________________________������IIΪһϵ�в����������Ǽ���Ũ������ȴ�ᾧ�������������õ����մ�������������___________��
��4��TiO2+��ˮ��������ˮ������ӷ���ʽΪ______________________����ת�������õ���TiO2+��ˮ���������Ҫ����Һ���ȣ����ȵ�Ŀ����________________________________��
��5�����������ĵ���ʹFe3+����FePO4������Һ��c(PO43-)= 1.0��10-17mol/Lʱ����ΪFe3+ ������ȫ������Һ��Fe3+������ȫʱ��c(Fe3+)=_______mol/L[��֪:���¶�����Ksp(FePO4)=1.0��10-22]��
��6���������������Ʊ�LiFePO4�Ĺ����У�����17% H2O2��Һ�����( H2C2O4)����������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����X����Һ�У�����Y�Լ��������ij��������������ͼ��ʾ�����������������������
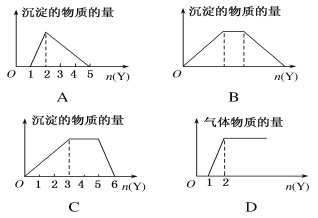
A. ��HCl��AlCl3�Ļ��Һ�еμ�NaOH��Һ
B. ��NaOH��Ca(OH)2�Ļ��Һ��ͨ��CO2
C. ��NH4Al(SO4)2��Һ�еμ�NaOH��Һ
D. ��NaOH��Na2CO3�Ļ��Һ�еμ�ϡ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com