
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.46 g有机物C2H6O中含有的H—O键的数目为NA
B.常温下,2 L 1 mol·L-1的乙酸溶液中,所含分子总数小于2NA
C.标准状况下,5.6 L NO和5.6 L O2组成的混合气体中所含原子数为NA
D.对于反应:C2H2(g)+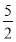 O2(g)=2CO2(g)+H2O(l)ΔH=-1300 kJ/mol,有2NA个碳氧双键形成时,放出1300 kJ的热量
O2(g)=2CO2(g)+H2O(l)ΔH=-1300 kJ/mol,有2NA个碳氧双键形成时,放出1300 kJ的热量
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案科目:高中化学 来源:2014年高二化学苏教版选修2 5.3无土栽培技术练习卷(解析版) 题型:选择题
在无土栽培中,需配制一定量含50 mol NH4Cl、16 mol KCl和24 mol K2SO4的营养液。若用KCl、NH4Cl和(NH4)2SO4三种固体为原料来配制,三者的物质的量依次是(单位为mol)( )。
A.2、64、24 B.64、2、24
C.32、50、12 D.16、50、24
查看答案和解析>>
科目:高中化学 来源:2014年高二化学苏教版选修2 4.2材料组成的优化练习卷(解析版) 题型:填空题
材料是人类生存和社会发展的物质基础,不同的材料功能各不相同。以下都是有关材料的内容,试根据所给内容回答问题。
(1)氢能是未来能源最佳选择之一,氢能的利用涉及氢的储存、输运和使用。贮氢合金是解决氢的储存等问题的重要材料。贮氢合金中最具代表的是镧?镍合金(LaNi5),已知LaNi5(s)+3H2(g) 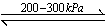 LaNi5H6(s)ΔH=-31.77 kJ·mol-1。
LaNi5H6(s)ΔH=-31.77 kJ·mol-1。
镧?镍合金的熔点比镧、镍的熔点________(填“高”“低”或“介于两者之间”),根据反应原理,形成LaNi5H6的化学反应条件是________。最近有人提出可以研制出一种性能优越的催化剂,可以大大提高贮氢合金的贮氢能力,你认为该讲法可信吗?________(填“可信”或“不可信”),其理由是___________________________________________________。
(2)无机非金属材料是日常生活中不可缺少的物质,它往往具有高强度、耐高温、耐腐蚀的特点。Si3N4就是一种重要的精细陶瓷,合成氮化硅的方法之一为:
3SiO2+6C+2N2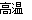 Si3N4+6CO。Si3N4属于________晶体,在上述反应中氧化剂为________。
Si3N4+6CO。Si3N4属于________晶体,在上述反应中氧化剂为________。
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题3氧化还原反应练习卷(解析版) 题型:选择题
在浓盐酸中H3AsO3与SnCl2反应的离子方程式为3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62—+6M。下列关于该反应的说法中,错误的是( )
A.M为H2O
B.每还原1 mol氧化剂,就有3 mol电子转移
C.还原性:SnCl2>As
D.氧化产物和还原产物的物质的量之比为2∶3
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题2化学常用计量练习卷(解析版) 题型:填空题
(1)下列实验操作或对实验事实的描述不正确的是________(填序号)。
A.不宜用瓷坩埚灼烧氢氧化钠或碳酸钠
B.使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏大
C.分液操作时,由于分液漏斗下端已沾满下层液体,故上层液体要从上口倒出
D.用托盘天平称量11.74 g氯化钠晶体
E.用结晶法分离硝酸钾和氯化钠的混合物
(2)实验室需要0.1 mol·L-1 NaOH溶液450 mL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
①如图所示的仪器中配制溶液肯定不需要的是________(填序号);配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
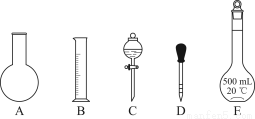
②下列操作中,容量瓶所不具备的功能有________(填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
③请计算需用托盘天平称取固体NaOH的质量为________g。某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图。由图中可以看出,烧杯的实际质量为________g。
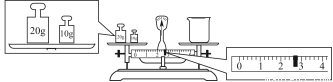
④根据计算得知,所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________mL(计算结果保留一位小数)。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是_____________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题2化学常用计量练习卷(解析版) 题型:选择题
下列叙述的两个量,一定相等的是( )
A.质量相等的金刚石和C60中的碳原子数目
B.0.1 mol/L NaCl溶液与0.05 mol/L Na2CO3溶液中所含Na+的数目
C.标准状况下等体积的SO2和SO3的分子数目
D.等体积pH都为3的稀盐酸与FeCl3溶液中,由水电离产生的H+数目
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题1物质的组成分类变化和用语练习卷(解析版) 题型:选择题
有关生活中常见的有机物的说法正确的是( )
A.汽油、苯、乙醇都属于烃类物质
B.油脂皂化后可用盐析的方法使高级脂肪酸钠和甘油分离
C.乙醇能被氧化成乙酸,两者都能与氢氧化钠溶液反应
D.煤的干馏可得煤油,甲烷、乙烯和苯能从石油分馏得到
查看答案和解析>>
科目:高中化学 来源:2014年高二化学苏教版选修2 3.3纤维素的化学加工练习卷(解析版) 题型:选择题
对于淀粉和纤维素两种物质,下列说法正确的是( )。
A.二者都能水解,且水解的最终产物相同
B.二者含C、H、O三种元素的质量分数相同,且互为同分异构体
C.它们都属于糖类,且都是高分子化合物
D.都可用(C6H10O5)n表示,但淀粉能发生银镜反应,而纤维素不能
查看答案和解析>>
科目:高中化学 来源:2014年高二化学苏教版选修2 2.3硫酸工业练习卷(解析版) 题型:填空题
钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域。V2O5是接触法制硫酸的催化剂。
(1)一定条件下,SO2与空气反应t min后,SO2和SO3物质的量浓度分别为a mol·L-1和b mol·L-1,则SO2起始物质的量浓度为________ mol·L-1;生成SO3的化学反应速率为________ mol·L-1·min-1。
(2)工业制硫酸,尾气SO2用________吸收。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com