
设阿伏加德罗常数的数值为NA,下列说法正确的是
A.11.2L氮气所含的分子数为0.5NA
B.16g CH4含有的电子数为8NA
C.7.8gNa2O2与足量CO2反应,转移的电子数为0.1NA
D.1L0.1molL-1的Na2S溶液中含有的S2-为0.1 NA
科目:高中化学 来源:2014-2015学年江西省鹰潭市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
分了式为C6H12O2并能与NaHCO3发生反应生成气体的有机物有x种(不包括立体异构,下同),分子式为C5H12O并能与Na发生反应的有机物有y种,则x和y的关系为
A.x=y B.x>y C.x<y D.无法确定
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三学业水平模拟考试化学试卷(解析版) 题型:选择题
对于反应2H2O2===2H2O+ O2↑,下列措施能加快该反应速率的是
A.减小压强 B.加热 C.加水稀释 D.降低温度
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三学业水平模拟考试化学试卷(解析版) 题型:选择题
用聚光手电筒照射下列分散系,可观察到丁达尔效应的是
A.KOH溶液 B.Fe(OH)3胶体 C.盐酸 D.NaNO3溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省湛江市高三普通高考测试(二)理综化学试卷(解析版) 题型:选择题
几种短周期元素的原子半径及主要化合价如下表,下列说法正确的是
元素代号 | X | Y | Z | M | R | Q | |
原子半径(×10-10 m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | —— |
最低负价 | —— | -1 | —— | —— | -3 | -2 | |
A.元素X和Q形成的化合物中只含有离子键
B.X、Z、R的最高价氧化物的水化物之间可两两相互反应
C.用单质Z做的容器不能盛装浓硫酸
D.Y的气态氢化物与R的气态氢化物能反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省揭阳市高三毕业班二模考试理综化学试卷(解析版) 题型:简答题
(16分)能源、环境与人类生活和社会发展密切相关,研究它们的综合利用有重要意义。
(1)氧化还原法消除氮氧化物的转化如下:
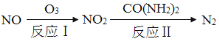
①反应I为:NO+O3=NO2+O2,生成11.2 L O2(标准状况)时,转移电子的物质的量是 mol。
②反应II中,当n(NO2)∶n[CO(NH2)2]=3∶2时,反应的化学方程式是 。
(2)硝化法是一种古老的生产硫酸的方法,同时实现氮氧化物的循环转化,主要反应为:
NO2(g)+SO2(g)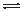 SO3(g)+NO(g) △H=-41.8 kJ·mol-1
SO3(g)+NO(g) △H=-41.8 kJ·mol-1
已知:2SO2(g)+O2(g)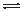 2SO3(g) △H=-196.6 kJ·mol-1。
2SO3(g) △H=-196.6 kJ·mol-1。
写出NO和O2反应生成NO2的热化学方程 式 。
(3)将燃煤废气中的CO2转化为二甲醚的反应原理为:
2CO2(g)+6H2(g)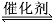 CH3OCH3(g)+3H2O(g);该反应 平衡常数表达式为K= 。
CH3OCH3(g)+3H2O(g);该反应 平衡常数表达式为K= 。
(4)合成气CO和H2在一定条件下能发生如下反应:
CO(g) +2H2(g) CH3OH(g) △H<0。
CH3OH(g) △H<0。
在容积均为V L的I、II、III三个相同密闭容器中分别充入a mol CO和2a mol H2,三个容器的反应温度分别为T1、T2、T3且恒定不变,在其他条件相同的情况下,实验测得反应均进行到t min时CO的体积分数υ(CO)%如图所示,
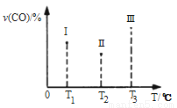
此时I、II、III三个容器中一定达到化学平衡状态的是 ;若三个容器内的反应再经过一段时间后都达到化学平衡时,CO转化率最大的反应温度是 。
(5)据报道以二氧化碳为原料,采用特殊的电极电解强酸性的二氧化碳水溶液可得到多种燃料,其原理如下图所示。电解时,b极上生成乙烯的电极反应式为___________________.

查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省揭阳市高三毕业班二模考试理综化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中能大量共存的是
A.pH=l的溶液中:Mg2+、Na+、AlO2-、SO42-
B.含有0.1 mol·L-1 Fe3+的溶液中:K+、Mg2+、I-、NO3-
C.含有大量NO3-的溶液中:H+、Na+、Fe3+、Cl-
D.含有大量Al3+的溶液中:Ca2+、K+、Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省成都市高三4月模拟考理综化学试卷(解析版) 题型:实验题
黄铁矿是工业上制取硫酸的主要原料,其主要成分为FeS2,含少量杂质(杂质不含S元素,且高温下不反应)。某化学兴趣小组用下列装置测定黄铁矿中硫元素的质量分数。
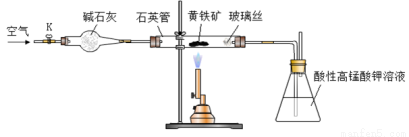
称取2.0g研细的黄铁矿样品,将样品放入石英管中,缓慢鼓入空气,再加热石英管至800~850℃;锥形瓶中盛装100 mL 0.2mol/L酸性KMnO4溶液用于吸收SO2(忽略SO2、H2SO3与氧气反应);反应结束后,每次从锥形瓶中取出25.00 mL溶液,用0.23mol/L标准H2C2O4溶液滴定,重复三次。
已知:4FeS2+11O2 2Fe2O3+8SO2;
2Fe2O3+8SO2;
2KMnO4+5SO2+2H2O K2SO4+2MnSO4+2H2SO4
K2SO4+2MnSO4+2H2SO4
请回答下列问题:
(1)连接好装置,检查装置气密性的操作是 。
(2)通入空气的作用是 。
(3)若实验过程中鼓入空气的速率过快,则测得的硫元素的质量分数 (填“偏高”、“偏低”或“不变”)。
(4)滴定时,应选择图中的 (填字母序号)盛装标准H2C2O4溶液,根据 现象来判断滴定已经达到终点。

(5)滴定过程中发生反应的离子方程式是 。
(6)如果黄铁矿中的硫全部转化为SO2,且被酸性KMnO4溶液完全吸收,滴定操作中,平均耗用0.23mol/L标准H2C2O4溶液21.73mL,则黄铁矿样品中硫元素的质量分数是 (保留到小数点后1位)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市高三下学期二模考试理综化学试卷(解析版) 题型:选择题
已知废旧干电池中的填充物主要有二氧化锰、炭黑、氯化锌、氯化铵、淀粉糊、Mn2O3、ZnO、FeO、汞的化合物等。某实验小组的同学拟回收废旧电池中的部份物质,主要操作流程如下图:
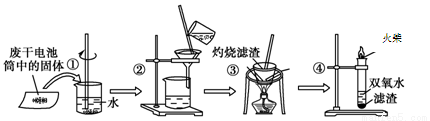
下列说法不正确的是
A. 步骤①②的名称分别为溶解、过滤
B. 步骤③中使用的化学仪器有酒精灯、三角架、泥三角、坩埚、玻璃棒
C. 步骤①②③中都使用了玻璃棒,且三个操作中玻璃棒的作用不完全相同
D. 步骤④的离子方程式为2Fe2++2H++H2O2 = 2Fe3++2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com