
下列说法错误的是
A.化学键的断裂和形成是化学反应中能量变化的主要原因
B.放热反应和吸热反应决定于反应物的总能量与生成物的总能量的相对大小
C.化学反应中能量变化,通常主要表现为热量的变化------放热或者吸热
D.凡经加热而发生的化学反应都是吸热反应
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源:2015届海南省高三第四次月考化学试卷(解析版) 题型:选择题
向含有FeCl3、BaCl2的酸性溶液中通入SO2气体会有沉淀产生,该沉淀是
A.BaSO4 B.FeS C.BaSO3 D.S
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三上学期回头考试化学试卷(解析版) 题型:选择题
右图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系。该溶液的成分可能是 ( )

A.NH4Al(SO4)2 B.KAl(SO4)2
C.Al2(SO4)3 D.NaAlO2
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高三第一次联考化学试卷(解析版) 题型:选择题
将某些化学知识用图像表示,可以收到直观、简明的效果。下列图象所表示的化学知识中,不正确的是
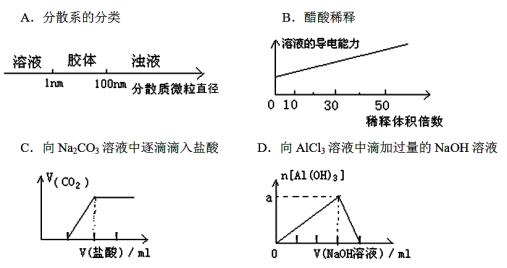
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高三第一次联考化学试卷(解析版) 题型:选择题
下列关于离子共存的评价及离子方程式书写正确的是
选项 | 离子组 | 评价 |
A | H+、Mg2+、Br-、NO3- | 能大量共存于同一溶液中,投入少量锌粉后,可放出H2 ,反应的离子方程式为 Zn+ 2H+ = Zn2++ H2↑ |
B | NH4+、CO32-、Cl-、Al3+ | 不能大量共存于同一溶液中,因为有沉淀生成 2Al3++3CO32-=Al2(CO3)3↓ |
C | ClO-、Na+、K+、HSO3- | 能大量共存于同一溶液中 |
D | HCO3-、OH-、Na+、K+ | 不能大量共存于同一溶液中,因为发生如下反应 HCO3-+ OH-= CO32-+ H2O |
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高三上学期期中联考化学试卷(解析版) 题型:填空题
(本题共15分)二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某学生拟有左下图所示的装置模拟制取并收集ClO2。

(1)B必须放在冰水浴中控制温度,其原因是 ;
(2)反应后在装置C中可得NaClO2溶液。已知NaClO2饱和溶液中在温度低于38℃时析出晶体是NaClO2·3H2O,在温度高于38℃时析出晶体是NaClO2。根据右上图所示的NaClO2的溶解度曲线,请补充从NaClO2溶液中制得NaClO2的操作步骤:
a ;b ;③洗涤;④干燥。
(3)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样;量取V1 mL试样加入到锥形瓶中;
步骤2:调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入淀粉指示剂,用c mol·L—1 Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。
(已知2 Na2S2O3 + I2 →Na2S4O6 + 2NaI)
①配制70 mL c mol/LNa2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有: 。
②步骤2中发生反应的离子方程式为: 。
③判断滴定终点的现象 。
原ClO2溶液的浓度为 g / L(用步骤中的字母代数式表示)。
④若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果 ;若滴定开始仰视读数,滴定终点时正确读数,则测定结果 。(填 “偏高”“偏低”或“不变”)
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高三上学期期中联考化学试卷(解析版) 题型:选择题
已知反应X (g) + Y (g)  n Z (g) △H > 0,将X和Y以一定比例混合通入密闭容器中进行反应,各物质的浓度随时间的改变如图所示。下列说法不正确的是( )
n Z (g) △H > 0,将X和Y以一定比例混合通入密闭容器中进行反应,各物质的浓度随时间的改变如图所示。下列说法不正确的是( )

A.反应方程式中n = 1
B.10 min时,曲线发生变化的原因是升高温度
C.10 min时,曲线发生变化的原因是增大压强
D.0~5 min内,用X表示的反应速率为v(X) = 0.08 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三9月月考化学试卷(解析版) 题型:填空题
(6分)由稀有气体元素Xe(氙)形成的一种共价化合物XeO3极不稳定,易转化为单质而呈强氧化性。将适量的XeO3投入30 mL Mn2+浓度为0.1 mol·L-1的水溶液中,刚好完全反应,放出的唯一气体是Xe单质,其在标准状况下的体积为56 mL,在反应过程中溶液的pH不断减小。
(1)已知Mn2+在不同条件下,可被氧化为+4、+6、+7等不同价态,依据题目所给出的数据推算氧化产物中锰元素的化合价为____________。
(2)试写出有关的离子方程式:________________。
(3)若将反应后的溶液稀释至90 mL,则稀释后溶液的pH为____________。
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三月考(10月)化学试卷(解析版) 题型:选择题
下列推论正确的是
A.在粗硅的制取中发生反应2C+SiO2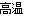 2CO↑+Si,硅被还原,可推知碳的非金属性强于硅的非金属性
2CO↑+Si,硅被还原,可推知碳的非金属性强于硅的非金属性
B.由“HF比HCl稳定性好”,可推知HF比HCl沸点高
C.由“同温度下等浓度的Na2CO3溶液比Na2SO4溶液的pH大”,可推知C比S的非金属性弱
D.由“某过程发生化学键断裂”,可推知该过程发生了化学变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com