
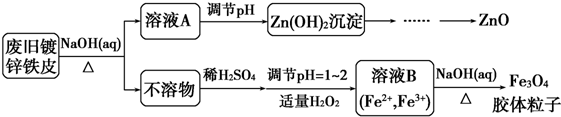
���� �Ͼɶ�п��Ƥ��������������Һ�з�Ӧ��п�ܽ�����ƫп���ƺ������������ܽ⣬���˵õ���ҺAΪNa2ZnO2��������ΪFe����ҺA����pHʹ��Һ��ZnO22-ת��ΪZn��OH��2�������پ������ˡ�ϴ�ӡ�������յõ�ZnO��������Fe�м������ᣬ��Ӧ��������������������ҺPH=1��2�������������������⣬����������������Ϊ�����ӣ��õ���Fe2+��Fe3+��B��Һ���ټ�������������Һ�����ȷֽ����������������������ӣ��Դ������
��� �⣺�ɶ�п��Ƥ��������������Һ�з�Ӧ��п�ܽ�����ƫп���ƺ������������ܽ⣬���˵õ���ҺAΪNa2ZnO2��������ΪFe����ҺA����pHʹ��Һ��ZnO22-ת��ΪZn��OH��2�������پ������ˡ�ϴ�ӡ�������յõ�ZnO��������Fe�м������ᣬ��Ӧ��������������������ҺPH=1��2�������������������⣬����������������Ϊ�����ӣ��õ���Fe2+��Fe3+��B��Һ���ټ�������������Һ�����ȷֽ����������������������ӣ�
��1��Fe3O4�ɿ���FeO��Fe2O3������Fe3O4����Ԫ�صĻ��ϼ���+2��+3�ۣ�Fe3O4��ϡH2SO4��Ӧ�Ļ�ѧ����ʽΪFe3O4+4H2SO4�TFeSO4+Fe2��SO4��3+4H2O��
�ʴ�Ϊ��+2��+3�ۣ�Fe3O4+4H2SO4�TFeSO4+Fe2��SO4��3+4H2O��
��2�������������£�H2O2�ܽ�Fe2+������Fe3+����Ӧ�����ӷ���ʽΪ2Fe2++H2O2+2H+�T2Fe3++2H2O��
�ʴ�Ϊ��2Fe2++H2O2+2H+�T2Fe3++2H2O��
��3����ҺB�к���Fe2+��Fe3+���ڿ����еμ�NaOH��Һ���������ӷ�Ӧ�У�Fe3++3OH-�TFe��OH��3����Fe2++2OH-�TFe��OH��2����4Fe��OH��2+O2+2H2O�T4Fe��OH��3��
�ʴ�Ϊ��Fe3++3OH-�TFe��OH��3����Fe2++2OH-�TFe��OH��2����4Fe��OH��2+O2+2H2O�T4Fe��OH��3��
��4��֤����ҺB�к���Fe3+�ķ���Ϊ����ҺB�е��뼸��KSCN��Һ������Һ��ɺ�ɫ֤����Һ�к���Fe3+��
�ʴ�Ϊ������ҺB�е��뼸��KSCN��Һ������Һ��ɺ�ɫ֤����Һ�к���Fe3+��
��5���������Ӿ��л�ԭ�ԣ�����B��Fe2+�ķ���Ϊ����ˮ������KMnO4��Һ���飮��ȡ����B��Һ�ڽྻ�Թ��е��뼸����ˮ������ˮ��ɫ����֤����ҺB�к���Fe2+��
�ʴ�Ϊ��ȡ����B��Һ�ڽྻ�Թ��е��뼸����ˮ������ˮ��ɫ����֤����ҺB�к���Fe2+��
��6��Ҫ�������ϵ�ͨ��N2ԭ������N2�������£��ɷ�ֹFe2+���������ʴ�Ϊ����N2�������£��ɷ�ֹFe2+��������
���� ���⿼�����ʵ��Ʊ�ʵ�飬Ϊ��Ƶ���㣬�����Ʊ������еķ�Ӧ�����ʵļ���ͼ����Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��������ԭ��Ӧ��Ӧ�ã���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| Ԫ�ش��� | A | B | C | D | E |
| ԭ�Ӱ뾶/nm | 0.186 | 0.143 | 0.089 | 0.104 | 0.074 |
| ��Ҫ���ϼ� | +1 | +3 | +2 | +6��-2 | -2 |
| A�� | E2-��B3+����������������� | |
| B�� | ���Ӱ뾶��СA+��E2- | |
| C�� | ����������Ӧˮ����ļ���A��C | |
| D�� | �⻯����ȶ���H2D��H2E |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaHCO3��Һ�м��������Ba��OH��2��Һ��2HCO3-+Ba2++2OH-�TBaCO3?+2H2O+CO32- | |
| B�� | FeCl3��Һ��HI��Һ��Ӧ��2Fe3++2HI�T2Fe2++I2+2H+ | |
| C�� | ��AgCl����Һ�еμ�Na2S��Һ����ɫ������ɺ�ɫ��2AgCl+S2-�TAg2S��+2Cl- | |
| D�� | ʯ��ʯ����ᷴӦ��CaCO3+2H+�TCa2++CO2��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | �������� | C�� | ��ˮ�Ҵ� | D�� | ʯ��ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������ˮ��2O22-+2H2O�T4OH-+O2�� | |
| B�� | ��С�մ�����θ����ࣺCO32-+2H+�TCO2��+H2O | |
| C�� | ����ͭ��Ba��OH��2��Һ��Ӧ��Cu2++2OH-�TCu��OH��2�� | |
| D�� | ̼������������Ca��OH��2��Һ��Ӧ��Ca2++2HCO3-+2OH-�TCaCO3��+CO32-+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ�������ͭƬ�ϣ�Cu+2H+�TCu2++H2�� | |
| B�� | ��������Һ���Ȼ�����Һ��ϣ�Ba2++SO42-�TBaSO4�� | |
| C�� | �������ʯ��ʯ�ϣ�CaCO3+2H+�TH2CO3+Ca2+ | |
| D�� | ����ͭ�������ϣ�Cu2++SO42-�TCuSO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������������������������� | |
| B�� | ���ó���������ĵ�����������������оƬ | |
| C�� | ʵ�����ö������̺�Ũ���Ṳ����ȡ�������� | |
| D�� | ����������ҺҪʢ����ĥ�ڲ��������Լ�ƿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��Na+����c��HS-����c��OH-����c ��H2S�� | B�� | c ��Na+��+c ��H+��=c ��S2-��+c ��OH-��+c ��HS-�� | ||
| C�� | 2c ��Na+��=c ��S2-��+c ��H2S��+c ��HS-�� | D�� | c��Na+����c��S2-����c��OH-����c ��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cl2��SO2����ʹƷ����Һ��ɫ��˵�����߾��������� | |
| B�� | �ֱ����HCl��NH3����ƿ������ˮ�к�Һ���Ѹ��������˵�����߾�������ˮ | |
| C�� | Fe��ϡHNO3��Һ��ϡH2SO4��Һ��Ӧ�������ݲ�����˵������Ӧ��Ϊ�û���Ӧ | |
| D�� | ���ȷֱ�ʢ���Ȼ�狀͵����֧�Թܣ��Թܵײ���������٣�˵�����߾��������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com