
VA族的氮、磷、砷(As)等元素的化合物在科研和生产中有许多重要用途,请回答下列问题。
(1)砷的基态原子的电子排布式为 。
(2)N、P、As原子的第一电离能由大到小的顺序为 。
(3)NH3的沸点比PH3 高,原因是 ;PO43-离子的立体构型为 。
高,原因是 ;PO43-离子的立体构型为 。
(4)PH3分子中P原子采用 杂化。
(5)H3AsO4和H3A sO3是砷的两种含氧酸,请根据结构与性质的关系,解释H3AsO4比H3AsO3酸性强的原因 。
sO3是砷的两种含氧酸,请根据结构与性质的关系,解释H3AsO4比H3AsO3酸性强的原因 。
(6) CuCl2与氨水反应可形成配合物[Cu(NH3)4]Cl2,1mol该配合物中含有σ键的数目为 。
(1) 1s22s22p63s23p63d104s24p3
(2) N>P>As
(3) NH3分子间存在较强的氢键,而PH3分子间仅有较弱的范德华力 正四面体
(4) sp3杂化
(5)H3AsO4和H3AsO3可表示为(HO)3AsO和(HO)3As,H3AsO3中的As为+3价,而H3AsO4中的As为+5价,正电性更高,导致As-O-H中O的电子更向As偏移,更易电离出H+
(6) 16mol或16×6.02×1023个
【解析】(1)砷是33号元素,其核外电子排布为,1s22s22p63s23p63d104s24p3 ;
(2)非金属性越强,第一电离能越大,N>P>As;
(3)NH3分子间存在较强的氢键,而PH3分子间仅有较弱的范德华力;PO43-是AB4型分子,所以空间构型是正四面体 。
(4)P原子中孤对电子对数=(5-3)/2=1,即P采取的是sp3杂化。
(5)两种含氧酸即可改写为(HO)mROn),H3AsO4可表示为(HO)3AsO,H3AsO3可表示为(HO)3As,H3AsO4中n值大正电性强,导致As-O-H中O的电子更向As偏移,更易电离出H+,所以H3AsO4比H3AsO3酸性强。
(6)1mol配合物[Cu(NH3)4]Cl2中,1mol氨气中含有3molσ键,总共含有σ键的物质的量为:3mol×4=12mol,1mol该配合物中含有4mol配位键,所以含有的σ键的物质的量为:12mol+4mol=16mol,或者16×6.02×1023个。


科目:高中化学 来源:2014高考名师推荐化学--预测7 题型:选择题
用表示阿伏加德罗常数的数值,下列说法正确的是
A.1 mol Na2O2晶体中共含有个离子
B.0.1 molAlCl3完全水解转化为氢氧化铝胶体,生成0.1NA个胶粒
C.常温常压下,和混合气体含有个氧原子
D.电解法冶炼铝时每转移个电子,阳极生成氧气
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测5 题型:选择题
现有等物质的量的铜和银的混合物17.2克,与50.0mL的浓硝酸恰好完全反应,产生气体4.48L(标准状况),则下列说法正确的是
A.产生的气体是0.2molNO2
B.硝酸的物质的量浓度为12mol/L
C.反应中被还原和未被还原的硝酸物质的量之比为3:2
D.要使产生的气体恰好完全被水吸收需要通入氧气0.075mol
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测4 题型:选择题
下列实验正确且能达到目的是
A.溴水中存在着如下的平衡:Br2+H2O HBr+HBrO,若要使溴水的颜色变浅,可采取的措施是加入NaI晶体
HBr+HBrO,若要使溴水的颜色变浅,可采取的措施是加入NaI晶体
B.在温水瓶中加入Na2CO3溶液泡浸后加入盐酸能除去内壁CaSO4
C.用饱和的NaOH热溶液除去乙酸乙酯中的乙醇、乙酸
D.亚硫酸钠具有较强的还原性,检验亚硫酸钠试样是否变质:

查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测3 题型:简答题
沈阳理工大学在废旧电池回收处理现状研究报告中报道了一种湿法处理方法,以下是对废旧电池材料(含有Ni(OH)2、碳粉、氧化铁和铝箔等)进行资源回收所设计的实验流程

已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。
②已知实验温度时的溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O
③金属离子在该实验流程下完全沉淀的pH:
离子 | Al3+ | Fe3+ | Ni2+ |
pH | 5.2 | 4.1 | 9.7 |
回答下列问题:
(1)物质A 的作用是调节溶液的pH以除去杂质Fe3+和Al3+,以下最适合作为A物质的是________。
A.NiO B.盐酸 C.NaOH D.氨水
(2)滤渣②的主要成分是_________________________________。
(3)写出加入Na2C2O4 溶液反应的化学方程式: _____________。
(4)写出电解滤液③的阴极反应式___________________________。
检验电解滤液③时阳极产生的气体的方法是用湿润的________试纸检验。
(5)由沉淀A生成Ni(OH)3的过程是先在滤渣③中加入过量NaOH溶液进行沉淀转化,待反应完全后再通入电解滤液③产生的气体进行氧化,请写出该氧化过程的离子方程式:__________________。
(6)如何检验Ni(OH)3是否洗涤干净?
________________________________。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测3 题型:选择题
下列实验操作不能达到其对应目的的是
序号 | 实验内容 | 实验目的 |
A. | 向盛有10滴0.1 mol/L AgNO3溶液的试管中滴加0.1 mol/L NaCl溶液,至不再有沉淀生成,再向其中滴加0.1 mol/L Na2S溶液 | 证明AgCl沉淀能转化为溶解度更小的Ag2S沉淀 |
B. | 向2 mL甲苯中加入3滴KMnO4酸性溶液,振荡;向2mL己烷中加入3滴KMnO4酸性溶液,振荡 | 证明与苯环相连的甲基易被氧化 |
C. | 向Na2SiO3溶液中通入CO2 | 证明碳酸的酸性比硅酸强 |
D. | 在淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的氢氧化铜并加热 | 验证淀粉已水解 |
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测3 题型:选择题
乙醇与重铬酸根离子在酸性溶液中能发生如下反应:C2H5OH+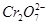 +H+—→CO2↑+Cr3++H2O,当这个方程式配平后,H+的化学计量数为
+H+—→CO2↑+Cr3++H2O,当这个方程式配平后,H+的化学计量数为
A.10
B.12
C.14
D.16
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测17 题型:推断题
甲酯除草醚(下图中E)是一种光合作用抑制剂,能被叶片吸收,但在植物体内传导速度较慢,它是芽前除草剂,主要用于大豆除草。某烃A合成E的路线如下:A
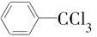
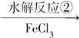
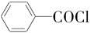
 B
B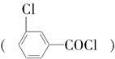

C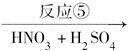 D
D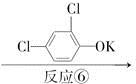

(1)写出A、C的结构简式:A________;C________。
(2)写出C中官能团的名称:________________。
(3)写出下列反应的化学方程式:
反应⑤______________________________________________________;
反应⑥__________________________________________________________,
反应类型是____________________________________________________。
(4)C的同分异构体有多种。写出核磁共振氢谱有四种不同化学环境的氢,且峰面积比为1∶2∶2∶2的四种有机物的结构简式: _________________________。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测15 题型:实验题
某同学在探究废干电池内的黑色固体回收利用时,进行如图所示实验:
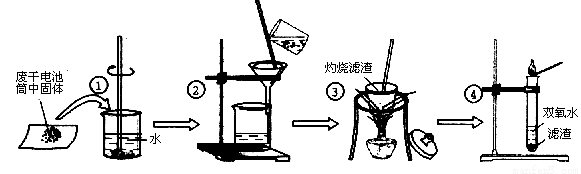
查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
(1)操作①的名称是 ;
(2)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、 、泥三角和三脚架;操作③灼烧滤渣中的黑色固体时,产生一种无色无味能使澄清石灰水变浑浊的气体,由此推测灼烧前的滤渣中存在的物质有 。
(3)往操作④的试管中加入操作③灼烧后所得黑色固体,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定灼烧后的黑色固体为 , 操作④相关的化学方程式为 。
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4+,该同学取少许滤液于试管中 (填写操作与现象),则证实滤液中含有NH4+。
(5)该同学利用在废旧干电池中回收的Zn片和石墨电极,设计一个原电池实验,比较铜与锌的金属活动性强弱。
限用材料:铜片、锌片、石墨电极、稀硫酸、CuSO4溶液、ZnSO4溶液;
限用仪器:直流电源、电流计、导线、烧杯、试管、盐桥等中学化学常见的药品和仪器
请画出实验装置图,并作相应标注,同时写出正极方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com