
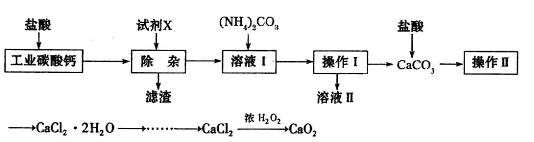
| A.CaO | B.CaCO3 | C.NH3·H2O | D.Ba(OH)2 |
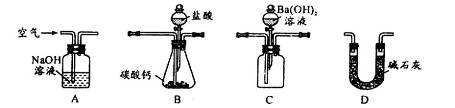
 ×100g/mol=9.00g,所以样品中CaCO3的质量分数为
×100g/mol=9.00g,所以样品中CaCO3的质量分数为 ×100%=90%。
×100%=90%。

科目:高中化学 来源:不详 题型:实验题
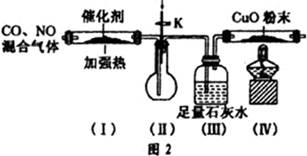
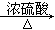 CO+H2O。实验室有如图l所示的装置,制取CO气体可选用的装置为
CO+H2O。实验室有如图l所示的装置,制取CO气体可选用的装置为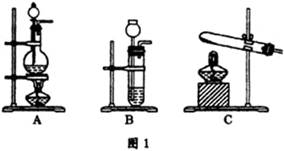
| 沉淀物 | Fe(OH)3 | Zn(OH)2 |
| pH | 1.5~3.2 | 6.4~8.0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

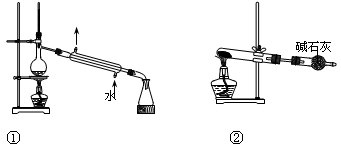
| A.①可用于分离苯和溴苯的混合物 | B.①可用于分离乙酸和乙醇的混合物 |
| C.②可用于分解NH4Cl制备NH3 | D.②可用于Ca(OH)2与NH4Cl共热制备NH3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 溴化钠溶液(NaI) | 氯水,CCl4 | 萃取、分液 |
| B | 苯(苯酚) | NaOH溶液 | 过滤 |
| C | CO2(HCl) | 饱和Na2CO3溶液 | 洗气 |
| D | 乙醇(乙酸) | 新制生石灰(CaO) | 蒸馏 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.用图1所示装置除去HCl中含有的少量Cl2 |
| B.用图2所示装置蒸发FeCl3溶液制备无水FeCl3 |
| C.用图3所示装置可以完成“喷泉”实验 |
| D.用图4所示装置制取并收集干燥纯净的NH3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
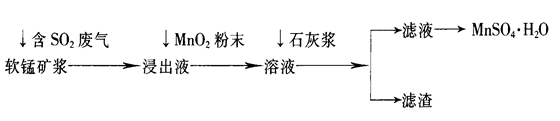
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| A.水 | B.硫酸 | C.氢氧化钠溶液 | D.氯化锶饱和溶液 |
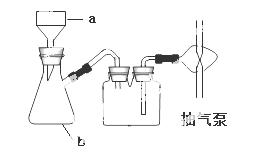
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
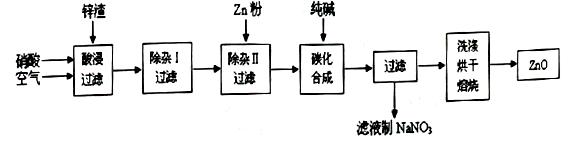
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 | 8.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com