
分析 (1)根据n=$\frac{m}{M}$计算出11.2gFe的物质的量,然后根据反应方程式Fe+2HCl=FeCl2+H2↑计算出生成氢气的物质的量;
(2)根据V(H2)=nVm计算出生成的氢气在标准状况下的体积.
解答 解:(1)11.2g金属铁的物质的量为:$\frac{11.2g}{56g/mol}$=0.2mol,
铁与盐酸恰好反应,所得溶液为氯化亚铁溶液,设反应生成氢气的物质的量为xmol,则:
Fe+2HCl=FeCl2+H2↑
1 1
0.2mol x
即$\frac{1}{0.2mol}$=$\frac{1}{x}$,解得:x=0.2mol,
答:生成氢气的物质的量为0.2mol;
(2)标准状况下0.2mol氢气的体积为:V(H2)=nVm=0.2mol×22.4L/mol=4.48L,
答:生成的氢气在标准状况下的体积为4.48.
点评 本题考查了化学方程式的计算,题目难度中等,明确发生反应的原理为解答关键,注意掌握物质的量与摩尔质量、气体摩尔体积之间的关系,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 | |
| B. | 在未知溶液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存在SO42-或SO32- | |
| C. | 做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸.如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加 | |
| D. | 提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
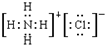 ;
;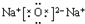 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锂在放电时做正极材料,充电时为阳极材料 | |
| B. | 电池在放电时,Li+向负极移动 | |
| C. | 该电池充电时阳极的反应为:LixV2O5-xe-=V2O5+xLi+ | |
| D. | V2O5只是锂发生反应的载体,不参与电池反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ③⑥⑦ | C. | ①③④ | D. | ③⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+、SCN-、CO32-、K+ | B. | SO32-、S2-、Al3+、Na+ | ||
| C. | NO3-、CH3COO-、Ba2+、Cl- | D. | SO42-、NH4+、ClO-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2mol/L | B. | 0.06 mol/L | C. | 0.12 mol/L | D. | 0.08mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com