
【题目】按要求回答下列问题:
(1)已知拆开![]() 键、
键、![]() 键、
键、![]() 键分别需要吸收的能量为
键分别需要吸收的能量为![]() 、
、![]() 、
、![]() 。则由
。则由![]() 和
和![]() 反应生成1molHCl需要_______
反应生成1molHCl需要_______![]() 填“放出”或“吸收”
填“放出”或“吸收”![]() _________
_________![]() 的热量。
的热量。
![]() 可以在
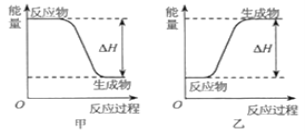
可以在![]() 中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图_____
中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图_____![]() 填“甲”或“乙”
填“甲”或“乙”![]() 。
。
(3)将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应 ![]() 。2min后,测得D的浓度为
。2min后,测得D的浓度为![]() mol/L ,
mol/L ,![]() ,C的反应速率是
,C的反应速率是![]() mol/(L·min)。则:
mol/(L·min)。则:
![]() 的值是__________;
的值是__________;
![]() 的平均反应速率是____________;
的平均反应速率是____________;
![]() 在2min末的浓度是________________;
在2min末的浓度是________________;
④若此后各物质的量均不再变化,则证明此可逆反应达到了_______的程度。
A.反应彻底 ![]() 反应终止
反应终止 ![]() 化学平衡
化学平衡 ![]() 无法判断
无法判断
【答案】放出 92.25 甲 2 0.125molL-1min-1 0.75mol/L C
【解析】
(1)依据焓变△H=反应物的化学键键能之和—生成物的化学键键能之和计算;
(2)H2可以在Cl2中安静地燃烧,该反应属于放热反应,据此判断;
(3)①根据v=![]() 计算出v(D),结合反应速率与化学计量数成正比计算x;②结合v(B)=
计算出v(D),结合反应速率与化学计量数成正比计算x;②结合v(B)=![]() v(D)计算;③经5min后D的浓度为0.5mol/L,D的物质的量为:2L×0.5mol/L=1mol,设A、B的初始浓度为n,根据三段式计算出n,再根据c=
v(D)计算;③经5min后D的浓度为0.5mol/L,D的物质的量为:2L×0.5mol/L=1mol,设A、B的初始浓度为n,根据三段式计算出n,再根据c=![]() 计算;④根据平衡状态的特征分析判断。
计算;④根据平衡状态的特征分析判断。
(1)已知拆开1molH-H键、1molCl-Cl键、1molH-Cl键分别需要的能量是436.4kJ、242.7kJ、431.8kJ,则反应:H2(g)+Cl2(g)=2HCl(g)的△H=436.4kJ/mol+242.7kJ/mol-2×431.8kJ/mol=-185.5kJ/mol,反应生成1molHCl需要放出92.25kJ的热量,故答案为:放出;92.25;
(2)H2可以在Cl2中安静地燃烧,该反应属于放热反应,反应物的总能量大于生成物的总能量,能表示该反应能量变化的是图甲;故答案为:甲;
(3)①经2min后,测得D的浓度为0.5mol/L,v(D)=![]() =0.25 mol/(Lmin),反应速率之比等于化学计量数之比,所以v(D)∶v(C)=0.25 mol/(Lmin)∶0.25mol/(Lmin)=2∶x,解得:x=2,故答案为:2;
=0.25 mol/(Lmin),反应速率之比等于化学计量数之比,所以v(D)∶v(C)=0.25 mol/(Lmin)∶0.25mol/(Lmin)=2∶x,解得:x=2,故答案为:2;
②v(D)=0.25 mol/(Lmin),则v(B)= ![]() v(D)=0.25 mol/(Lmin)×
v(D)=0.25 mol/(Lmin)×![]() =0.125 mol/(Lmin),故答案为:0.125 mol/(Lmin);
=0.125 mol/(Lmin),故答案为:0.125 mol/(Lmin);
③经2min后D的浓度为0.5mol/L,D的物质的量为:2L×0.5mol/L=1mol,设A、B的初始浓度为n,
3A(g) + B(g) ![]() 2C(g)+2D(g)
2C(g)+2D(g)
起始(mol) n n 0 0
变化(mol) 1.5 0.5 1 1
5min(mol) n-1.5 n-0.5 1 1
c(A)∶c(B)= n(A)∶n(B)= ![]() =3∶5,解得:n=3,2min末A的浓度为:
=3∶5,解得:n=3,2min末A的浓度为:![]() =0.75mol/L,故答案为:0.75mol/L;
=0.75mol/L,故答案为:0.75mol/L;
④若此后各物质的量均不再变化,则证明此可逆反应达到了化学平衡状态,也就达到了该反应的化学反应限度,故选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】化学与生活息息相关,以下做法不正确的是( )
A. 集中处理废旧电池,以防止重金属污染
B. 食用含铁丰富的食物,可预防缺铁性贫血
C. 使用加碘食盐,可预防因缺碘引起的甲状腺肿大
D. 大量使用食品添加剂,可使食品营养更丰富
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产水煤气的反应为:C(s)+H2O(g)![]() CO(g)+H2(g) ΔH=+131.4kJ·mol-1下列判断正确的是
CO(g)+H2(g) ΔH=+131.4kJ·mol-1下列判断正确的是
A. 反应物能量总和大于生成物能量总和
B. CO(g)+H2(g)![]() C(s)+H2O(g)ΔH=+131.4kJ·mol-1
C(s)+H2O(g)ΔH=+131.4kJ·mol-1
C. 水煤气反应中,生成1 mol H2(g)吸收131.4 kJ热量
D. 水煤气反应中生成1体积CO(g)吸收131.4 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大。其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同。X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子。根据以上叙述,下列说法中一定正确的是( )
A. 元素非金属性比较为:![]()
B. W、X、Y、Z原子的核外最外层电子数的总和为20
C. W与Y可形成既含极性共价键又含非极性共价键的化合物
D. 由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一处于平衡状态的反应:X(s)+3Y(g)![]() 2Z (g),ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是
2Z (g),ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是
①高温 ②低温 ③高压 ④低压 ⑤加催化剂 ⑥分离出Z
A. ①③⑤ B. ②③⑤ C. ②③⑥ D. ②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表示氢气燃烧热的是( )
A. H2(g) + 1/2O2(g)=H2O(g) △H=-241.8 kJ/mol
B. 2H2(g) + O2(g)=2H2O(g) △H=-483.6 kJ/mol
C. H2(g) + 1/2O2(g)=H2O(l) △H=-285.8 kJ/mol
D. 2H2(g) + O2(g)=2H2O(l) △H=-571.6 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在 2A(g) + B(g) 3C(g) + 4D(g)反应中,下面表示的反应速率最快的是
A. v (A)=0.5mol/(Ls) B. v (B)=1.8 mol/(Lmin)
C. v (C)=0.8mol/(Ls) D. v (D)=1.0 mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y中含有相同的元素,Z、W中也含有相同的元素,根据反应X+H2O→Y+H2↑;Z+H2O→W+O2↑(方程式均未配平),可推断X、Y中及Z、W中相同元素的化合价的高低顺序为 ( )
A. X>Y,Z>W B. X<Y,Z<W
C. X>Y,Z<W D. X<Y,Z>W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g) === xC(g)+2D(g);5 min后测得c(D)=0.5 mol·L-1,c(A)∶c(B)=3∶5,C的反应速率是0.1 mol·L-1·min-1。
(1)A在5 min末的浓度是____________;
(2)v(B)=____________;
(3)x=____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com