
【题目】维生素C又叫抗坏血酸,是一种水溶性维生素,只含有C、H、O三种元素,其球棍模型如图所示。下列关于维生素C的说法正确的是( )
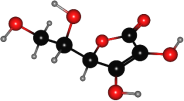
A.维生素C的分子式C6H8O6
B.维生素C含有1个手性碳原子
C.维生素C不能使溴水褪色
D.1mol维生素C与足量的钠反应能产生2molH2
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)是一种重要的化工试剂,氯化法是合成硫酰氯(SO2Cl2)的常用方法。实验室合成硫酰氯的实验装置如下图所示(部分夹持装置未画出):

已知:① SO2(g) + Cl2(g)=SO2Cl2(l) ΔH=-97.3 kJ/mol。
② 硫酰氯常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”。
③ 100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气。
回答下列问题:
(1) 装置A中发生反应的离子方程式为___________。
(2) 装置B的作用为_______________________________,若缺少装置C,装置D中SO2与Cl2还可能发生反应的化学方程式为________________________。
(3) 仪器F的名称为_________________,E中冷凝水的入口是___________(填“a”或“b”),F的作用为_______________________________________________。
(4) 当装置A中排出氯气1.12 L(已折算成标准状况)时,最终得到5.4 g纯净的硫酰氯,则硫酰氯的产率为____________。为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有________(填序号)。
① 先通冷凝水,再通气② 控制气流速率,宜慢不宜快
③ 若三颈烧瓶发烫,可适当降温④ 加热三颈烧瓶
(5) 氯磺酸(ClSO3H)加热分解,也能制得硫酰氯2ClSO3H=SO2Cl2 + H2SO4,分离产物的方法是_____
A.重结晶B.过滤 C.蒸馏D.萃取
(6) 长期存放的硫酰氯会发黄,其原因可能为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲和乙均是双液原电池装置,下列说法不正确的是( )
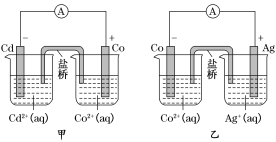
A. 甲中电池总反应的离子方程式为Cd(s)+Co2+(aq)=Co(s)+Cd2+(aq)
B. 盐桥的作用是形成闭合回路,并使两边溶液保持电中性
C. 反应2Ag(s)+Cd2+(aq)=Cd(s)+2Ag+(aq)能够发生
D. 乙电池中有1mol电子通过外电路时,正极有1mol Ag析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物丙可由如下反应得到
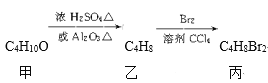
丙的结构简式不可能是( )
A. CH3CH(CH2Br)2B. (CH3)2CBrCH2Br
C. C2H5CHBrCH2BrD. CH3(CHBr)2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中化合物B既能使溴水褪色,又能溶解碳酸钙,D、E均为高分子化合物。根据下图填空:

(1)写出葡萄糖与新制氢氧化铜浊液反应的化学方程式:_____。
(2)A中的官能团有_____(写结构简式)。
(3)E在自然界中可降解,对环境无害,下列说法正确的是___。
A.由A生成E的反应属于加聚反应
B.E的相对分子质量为72
C.E用作一次性快餐盒有助于减少白色污染
(4)在反应①-⑤中,属于取代反应的是_____。写出D和F的结构简式:D_______,F_______。
(5)A跟氢氧化钙作用可制得一种常用的人体补钙剂,测得这种补钙剂的纯净物中钙元素的质量分数为13.0%,其结晶水的含量为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将15mL 1.0mol/L的CH3COOH(Ka=1.8×10-5)加入到5mL 2.0mol/L的NaOH溶液中,并将混合溶液稀释至100mL,则制得的溶液pH值约为
A. 4.4B. 4.8
C. 5.0D. 5.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐中常含有少量K+、Ca2+、Mg2+、![]() 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:
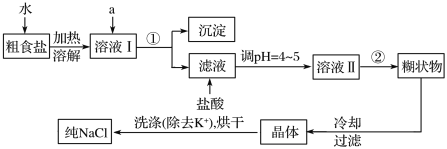
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液
(1)欲依次除去溶液Ⅰ中的Mg2+、![]() 、Ca2+,选出a所代表的试剂,按滴加顺序依次为_______溶液、_________溶液、_________溶液。(填化学式)。
、Ca2+,选出a所代表的试剂,按滴加顺序依次为_______溶液、_________溶液、_________溶液。(填化学式)。
(2)分离操作①中所用到的玻璃仪器除了玻璃棒,烧杯,还需要__________________。
(3)加盐酸的作用__________________
(4)实验室里将粗盐制成精盐的过程中,在溶解的操作中要用到玻璃棒,其作用为__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取Fe(OH)3胶体的方法是把______逐滴加在_______中,继续煮沸,待溶液呈____ 色时停止加热,其反应的离子方程式为_______________,用 __________(方法)可证明胶体已经制成,用_____方法精制胶体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com