
| n |
| V |
| 4.48L |
| 22.4L/mol |
| 0.8mol |
| 0.2L |


科目:高中化学 来源: 题型:
| A、①②④⑥ | B、②③④⑤ |
| C、①③④ | D、②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物.下列说法正确的是( )
霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物.下列说法正确的是( )| A、MMF能溶于水 |
| B、1 mol MMF能与含3 mol NaOH的水溶液完全反应 |
| C、1 mol MMF能与6 mol氢气发生加成反应 |
| D、MMF能发生取代反应和消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
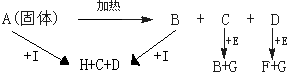
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
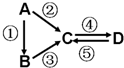 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如图的反应关系:查看答案和解析>>
科目:高中化学 来源: 题型:
 从某些植物树叶提取的挥发油中含有下列主要成分:
从某些植物树叶提取的挥发油中含有下列主要成分:查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | E | F | G | |||
| 实 验 仪 器 及 装 置 |  | 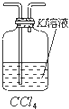 | 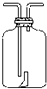 干燥红布条 | 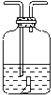 红布条水 |  饱和食盐水 | 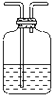 浓H2SO4 | 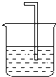 NaOH溶液 | ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com