
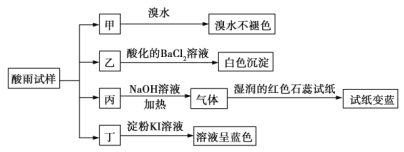
【题目】某地环保部门将收集到的一定量酸雨试样分成甲、乙、丙、丁四份,进行如图所示的实验探究。
已知酸雨试样中可能含有下表所示的某些离子:
阳离子 |
|
阴离子 |
|
请回答下列问题:
(1)![]() 是______,
是______,![]() 是______。
是______。
(2)可能存在的阴离子是______,能证明该阴离子是否存在的简单实验操作为______。
(3)写出丁试样中滴加淀粉![]() 溶液所发生反应的离子方程式:______。
溶液所发生反应的离子方程式:______。
(4)某次降雨收集到![]() 雨水,向雨水中滴加
雨水,向雨水中滴加![]() 的
的![]() 溶液,充分反应后测得溶液中
溶液,充分反应后测得溶液中![]() ,再向该溶液中加入足量的
,再向该溶液中加入足量的![]() 溶液,经过滤、蒸干、称重,测得沉淀的质量为
溶液,经过滤、蒸干、称重,测得沉淀的质量为![]() 。假设雨水的酸性仅由
。假设雨水的酸性仅由![]() 和
和![]() 的排放所致,则排放到空气中的
的排放所致,则排放到空气中的![]() 和
和![]() 的物质的量之比约为______(不考虑
的物质的量之比约为______(不考虑![]() 的相互反应)。
的相互反应)。
【答案】![]()
![]()
![]() 取少量酸雨试样,滴加足量的
取少量酸雨试样,滴加足量的![]() 溶液,静置,取上层清液,滴加
溶液,静置,取上层清液,滴加![]() 溶液,若有白色沉淀产生,则存在
溶液,若有白色沉淀产生,则存在![]() ;若无由色沉淀产生,则不存在
;若无由色沉淀产生,则不存在![]()
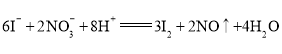
![]()
【解析】
酸雨试样加入溴水,溴水不褪色,说明酸雨试样不含还原性离子,所以不含![]() ;
;
酸雨试样加入氢氧化钠并加热,有氨气放出,说明酸雨试样中含有![]() ;酸雨试样加入淀粉碘化钾,溶液变蓝,说明有碘单质生成,酸雨试样含有氧化性离子,所以酸雨试样中含有
;酸雨试样加入淀粉碘化钾,溶液变蓝,说明有碘单质生成,酸雨试样含有氧化性离子,所以酸雨试样中含有![]() ;酸雨试样加入BaCl2溶液生成白色沉淀,说明酸雨试样含有
;酸雨试样加入BaCl2溶液生成白色沉淀,说明酸雨试样含有![]() ;
;
(1)根据以上分析,溶液中一定含有![]() 、
、![]() 、
、![]() ,一定不含
,一定不含![]() ;所以
;所以![]() 是
是![]() ,
,![]() 是
是![]() 。
。
(2)根据以上分析,可能存在的阴离子是![]() ,
,![]() 与银离子反应生成难溶于硝酸的白色沉淀氯化银,能证明
与银离子反应生成难溶于硝酸的白色沉淀氯化银,能证明![]() 是否存在的简单实验操作为:取少量酸雨试样,滴加足量的
是否存在的简单实验操作为:取少量酸雨试样,滴加足量的![]() 溶液,静置,取上层清液,滴加
溶液,静置,取上层清液,滴加![]() 溶液,若有白色沉淀产生,则存在
溶液,若有白色沉淀产生,则存在![]() ;若无由色沉淀产生,则不存在
;若无由色沉淀产生,则不存在![]() 。
。
(3)酸雨试样加入淀粉碘化钾,溶液变蓝,说明碘离子被硝酸氧化为碘单质,试样中滴加淀粉![]() 溶液所发生反应的离子方程式是
溶液所发生反应的离子方程式是![]() 。
。
(4)![]() 雨水,向雨水中滴加
雨水,向雨水中滴加![]() 的
的![]() 溶液,亚硫酸根离子被氧化为硫酸根离子,充分反应后测得溶液中
溶液,亚硫酸根离子被氧化为硫酸根离子,充分反应后测得溶液中![]() ,再向该溶液中加入足量的
,再向该溶液中加入足量的![]() 溶液,经过滤、蒸干、称重,生成硫酸钡沉淀的质量为
溶液,经过滤、蒸干、称重,生成硫酸钡沉淀的质量为![]() ,硫酸钡的物质的量是
,硫酸钡的物质的量是![]() 0.0008mol,硫酸的浓度为
0.0008mol,硫酸的浓度为![]() =
=![]() ,氢离子由硫酸、硝酸共同提供,所以硝酸的浓度是
,氢离子由硫酸、硝酸共同提供,所以硝酸的浓度是![]() ,则排放到空气中的
,则排放到空气中的![]() 和
和![]() 的物质的量之比约为1:1。
的物质的量之比约为1:1。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】将1.92g铜粉与一定量的浓硝酸反应,当铜粉完全作用时收集到气体1.12L(标准状况下),则消耗硝酸的物质的量是
A.0.12molB.0.09molC.0.11molD.0.08mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物0.3克完全燃烧后生成224毫升(标准状况)二氧化碳和0.18克水。已知该物质的蒸气对氢气的相对密度为30,试求:
(1)有机物的分子式___________
(2)试写出该有机物可能的结构简式并命名____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为检验某溶液中是否含有常见的四种无机离子,进行了如图所示的实验操作.其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝.由该实验能得到的正确结论是![]()
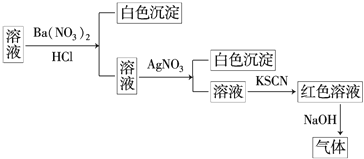
A.原溶液中一定含有![]() B.原溶液中一定含有
B.原溶液中一定含有![]()
C.原溶液中一定含有![]() D.原溶液中一定含有
D.原溶液中一定含有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有某稀硫酸和稀硝酸的混合溶液200 mL,将其平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g铜粉;向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化关系如图所示(假设硝酸的还原产物为NO气体)。下列分析或结果正确的是
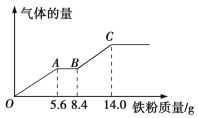
A. 原混合溶液中NO3-的物质的量为0.2 mol
B. OA段产生的是氢气
C. BC段产生NO
D. 原混合溶液中H2SO4的浓度为1.25mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有的离子可能是K+、Ba2+、Al3+、Mg2+、AlO2-、CO32-、SiO32-、Cl-中的几种,现进行如下实验:
①取少量溶液,加氢氧化钠溶液过程中无沉淀生成;
②另取少量原溶液,逐滴加入5mL0.2mol·L-1盐酸,产生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生气体,最后沉淀逐渐减少至消失;
③在上述②沉淀消失后的溶液中,再加入足量的硝酸银溶液可得到沉淀0.287g。
下列说法中正确的是( )
A.该溶液中一定不含Ba2+、Mg2+、Al3+、SiO32-、Cl-
B.该溶液中一定含有K+、AlO2-、CO32-、Cl-
C.该溶液是否有K+需做焰色反应实验(透过蓝色钴玻璃片)
D.可能含有Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如图所示。下列说法不正确的是
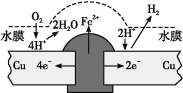
A.因铁的金属性比铜强,所以铁铆钉被氧化而腐蚀
B.若水膜中溶解了SO2,则铁铆钉腐蚀的速率变小
C.铜极上的反应是2H++2e =H2↑、O2+4e+4H+=2H2O
D.在金属表面涂一层油脂,能防止铁铆钉被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用中和滴定法测定一瓶烧碱溶液的浓度(该烧碱溶液中不含与酸反应的杂质),测定过程如下:
a.将锥形瓶置于酸式滴定管下,锥形瓶下垫一张白纸;
b.分别取25.00mL酸、碱滴定管各一支,洗涤并用待装液润洗;
c.打开酸式滴定管旋塞开始滴定直到终点,记录下终点时滴定管上的读数;
d.取一个用蒸馏水洗净的锥形瓶,从碱式滴定管中放出20.00mL待测碱液于锥形瓶中,滴入2至3滴酚酞试液;
e.碱式滴定管中加入待测烧碱溶液,酸式滴定管中加入0.1000mol·L-1的稀盐酸标准溶液,并将两支滴定管尖嘴部分的气泡均赶尽,记下液面刻度;
f.再重复上述操作2次。
三次测定获得的数据如下表:
实验次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前读数 | 滴定后读数 | ||
1 | 20.00 | 0.45 | 24.40 |
2 | 20.00 | 2.20 | 26.25 |
3 | 20.00 | 0.10 | 17.10 |
(1)上述实验操作的正确顺序是___(填字母序号)。
(2)实验中,除用酚酞作指示剂外,还可以选用___作该实验的指示剂,在锥形瓶下垫一张白纸的作用是___。
(3)如何判断滴定达到了终点?___
(4)根据实验数据,计算待测碱液的浓度为___mol·L-1(保留两位小数)。
(5)下列操作中可能使所测烧碱溶液的浓度数值偏低的是___。(填正确答案标号)
A.操作b中,未润洗酸式滴定管
B.操作e中,碱式滴定管尖嘴处的气泡未赶出,而取液后其尖嘴处的气泡消失了
C.操作d中,装碱液时,锥形瓶中还有少量蒸馏水
D.操作c中,滴定终点时发现酸式滴定管尖嘴处悬挂着一滴溶液
E.酸式滴定管读数时,滴定前仰视读数,滴定结束时俯视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体 X和气体Y各0.16mol充入 10L恒容密闭容器中,发生反应: X(g) + Y(g) 2Z(g) △ H < 0.一段时间后达到平衡,反应过程中测定的数据如表,下列说法正确的是( )

A.反应前 2 min 的平均速率v(Z) > 2.0 × 103 mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前:v(逆) > v(正)
C.保持其他条件不变,起始时向容器中充入0.32 mol气体 X和0.32 mol气体Y,到达平衡时,c(Z) > 0.24 mol·L-1
D.该温度下此反应的平衡常数:K = 1.44
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com