
��ͼ��ʾ�������ת����ϵ�У�����������ͷ�Ӧ��������ȥ������A��F��������ʽ�Σ�������B��C��Y��Z�����壬��B��ʹZ��ˮ��Һ��ɫ��E��һ�ֳ����Ļ��ʣ�X�к���20�����ӡ�
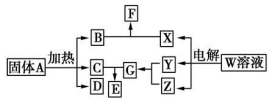
(1)д��X�ĵ���ʽ��________________ ��E�к��еĻ�ѧ��������________________��
(2)Z��C�����ʵ���֮��3?1��ӦҲ������G��ͬʱ������һ�ֶ�Ԫ������H����֪�÷�Ӧ��ֻ��һ��Ԫ�صĻ��ϼ۷����ı䣬��H�Ļ�ѧʽΪ________________��H����������۵�Ư������������ˮ��Ӧ�Ļ�ѧ����ʽΪ________________��
(3)�������Ϊ560 mL(��״��)��B��Zͬʱ����ͨ��ˮ�У��õ�1.0 L��Һ������Һ��c(H��)��________mol/L��
(4)A��G���������У����ڵ���ʵ���________�֡�
(1) ���ۼ������Ӽ�(�����ϡ���λ����Ҳ��ȷ)
���ۼ������Ӽ�(�����ϡ���λ����Ҳ��ȷ)
(2)NCl3��NCl3��3H2O===3HClO��NH3(��NCl3��4H2O===3HClO��NH3��H2O)
(3)0.1��(4)5
�����������⿼��������������ƶϡ�����ʡ���ѧ�����Լ���ѧ����ʽ����д��֪ʶ�����ڿ��鿼�������������ͷ��������������������֪��AΪNH4HSO3��BΪSO2��CΪNH3��DΪH2O��EΪNH4Cl��FΪNaHSO3��GΪHCl��WΪNaCl��XΪNaOH��YΪH2��ZΪCl2��(1)NaOH�ĵ���ʽΪ ��NH4Cl�м������Ӽ������й��ۼ���(2)�������⣬Z��C������Ӧ3Cl2��NH3===3HCl��NCl3��NCl3��ˮ������Ӧ����ѧ����ʽΪNCl3��3H2O===3HClO��NH3��(3)���������֪�������ʵ�����B��Zͬʱ����ͨ��ˮ�У�������ӦCl2��SO2��2H2O===4H����SO42-��2Cl����560 mL(��״��)����Ϊ0.025 mol�����ݷ�Ӧ����ʽ��֪������0.1 mol H����c(H��)��0.1 mol/L��(4)A��G���������У����ڵ���ʵ���NH4HSO3��H2O��NH4Cl��NaHSO3��HCl����5�֣�SO2��NH3Ϊ�ǵ���ʡ�
��NH4Cl�м������Ӽ������й��ۼ���(2)�������⣬Z��C������Ӧ3Cl2��NH3===3HCl��NCl3��NCl3��ˮ������Ӧ����ѧ����ʽΪNCl3��3H2O===3HClO��NH3��(3)���������֪�������ʵ�����B��Zͬʱ����ͨ��ˮ�У�������ӦCl2��SO2��2H2O===4H����SO42-��2Cl����560 mL(��״��)����Ϊ0.025 mol�����ݷ�Ӧ����ʽ��֪������0.1 mol H����c(H��)��0.1 mol/L��(4)A��G���������У����ڵ���ʵ���NH4HSO3��H2O��NH4Cl��NaHSO3��HCl����5�֣�SO2��NH3Ϊ�ǵ���ʡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��5 ���ͣ�ѡ����
��NA��ʾ�����ӵ�������ֵ��������������ȷ����
A��78 g ������̼̼˫������ĿΪ3NA
B�����³�ѹ�£�22.4 L������̼���е�ԭ������Ϊ3NA
C��1 mol Fe������ϡHNO3��Ӧ��ת��3 NA������
D��1 L 1 mol��L-1��NaClO ��Һ�к���ClO������ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��3 ���ͣ�ѡ����
������ʵ�����ý�����Խ��͵���
A�������п������Ƶ�ˮ����ˮ
B����п����Ʒ����Ʋ����ܱ�������Ʒ
C ����ҵ�ϳ����Ȼ�ԭ��ұ�������õ�ⷨұ����
����ҵ�ϳ����Ȼ�ԭ��ұ�������õ�ⷨұ����
D����ⷨ����ͭʱ���京�е�Ag��Au���ʳ����ڵ��۵ĵײ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��2 ���ͣ�ѡ����
��ѧ������������أ�����˵������ȷ����
A��PM2.5Ҳ��ϸ������Կ����������ܼ��ȵ�����Ҫ��Ӱ��
B��ϡ���������ᡢ�Ȼ�����Һ��������Ϊ����
C������ϩ������Ʒ������ʳƷ�İ�װ
D������������Һ�����ڻ���������ɱ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��17 ���ͣ��ƶ���
������A�Ǻϳ���Ȼ�ĵ��壬����ʽΪC5H8��A��һϵ�з�Ӧ���£����ַ�Ӧ������ȥ��
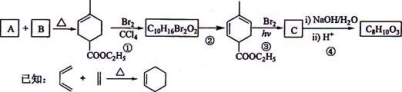
�ش��������⣺
��1��A�Ľṹ��ʽΪ��������������ѧ�����ǡ�����������
��2��B�ķ���ʽΪ����������
��3���ڵķ�Ӧ����ʽΪ�� ��
��4���ٺ͢۵ķ�Ӧ���ͷֱ��ǡ���������������������������
��5��CΪ�������������������Ǽ����ܵĻ�ѧ����ʽΪ ����6��A��ͬ���칹���в����ۼ�˫ϩ��C=C=C���ṹ��Ԫ����״�����С����֣�д�����л�Ϊ�����칹��Ļ�����Ľṹ��ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��17 ���ͣ�ѡ����
﮿��������һ�����͵Ķ��ε�أ���ŵ�ʱ�Ĺ���ԭ����ͼ��ʾ������˵����ȷ����
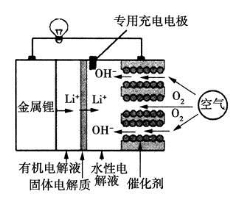
A���õ�طŵ�ʱ�������ķ�ӦʽΪO2��4e����4H��===2H2O
B���õ�س��ʱ������������������Ӧ��Li����e��===Li
C������е��л����Һ������ϡ�������
D��������������LiOH�ɻ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��16 ���ͣ�ѡ����
�������ӷ���ʽ��д��ȷ����
A����������Һ�еμӹ���Ũ��ˮ��Al3����4NH3��H2O===AlO2-��4NH4+ ��2H2O
B����������Һ�Լ��Ե�ԭ��CH3COO����H2O===CH3COOH��OH��
C������������Һ��������SO2���壺SO2��2OH��===SO32- ��H2O
D��Ư�۷����ڿ����б��ʣ�ClO����CO2��H2O===HClO��HCO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��14 ���ͣ�ѡ����
���������£������ܴ�������������ӷ���ʽ��ȷ���ǣ� ��
A��pH=1����Һ�У�Fe2+��ClO-��Na+��SO42-
B���ں��϶�Al3+����Һ�У�K+��Cl-��HCO3��
C��һС����Ͷ�뵽CuSO4��Һ�У�2Na��Cu2+= Cu��2Na+
D��ͭ����ϡ���3Cu + 8H+ + 2NO3- = 3Cu2++ 2NO��+ 4H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com