
【题目】甲型H1N1流感病毒曾在全球广泛传播,给人类健康、社会经济带来了巨大的负面影响。我国采取积极应对措施,使病毒得到了有效的控制,从很大程度上减少了损失,在这里,消毒液功不可没。
(1)生产消毒液是将氯气通入NaOH溶液中,该反应的离子方程式为________。
(2)取少量消毒液滴加AgNO3溶液,现象是出现白色沉淀,说明消毒液中有____离子(写离子符号),该反应的的离子方程式为____________。
(3)消毒液稀释后喷洒在空气中,可以生成具有漂白性的物质,该物质为_________;该物质有漂白性是因为它有强的氧化性,但是它也很不稳定,写出它分解反应的化学方程式:_________。
【答案】Cl2+2OH-=ClO-+Cl-+H2O Cl- Ag++Cl-= AgCl↓ HClO 2HClO![]() 2HCl+O2↑
2HCl+O2↑
【解析】
)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,次氯酸的酸性比碳酸弱,消毒液中的次氯酸钠与空气中二氧化碳反应生成次氯酸,次氯酸具有强氧化性,能起到杀菌消毒和漂白的作用。
(1)氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应的离子方程式为Cl2+2OH-=ClO-+Cl-+H2O,故答案为:Cl2+2OH-=ClO-+Cl-+H2O;
(2)向少量消毒液滴加AgNO3溶液,消毒液中的氯离子与银离子反应生成白色氯化银沉淀,反应的离子方程式为Ag++Cl-= AgCl↓,故答案为:Cl-;Ag++Cl-= AgCl↓;
(3)次氯酸的酸性比碳酸弱,消毒液稀释后喷洒在空气中,消毒液中的次氯酸钠与空气中二氧化碳反应生成次氯酸,次氯酸具有强氧化性,能起到杀菌消毒和漂白的作用,次氯酸不稳定,遇光易分解生成盐酸和氧气,反应的化学方程式为2HClO![]() 2HCl+O2↑,故答案为:HClO ;2HClO
2HCl+O2↑,故答案为:HClO ;2HClO![]() 2HCl+O2↑。
2HCl+O2↑。


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】短周期元素a、b、c、d的原子序数依次增大,a和b的最外电子数之和等于c和d的最外层电子数之和,这四种元素组成两种盐b2da3和bca2。在含该两种盐的混合溶液中滴加盐酸,产生白色沉淀的物质的量与盐酸体积的关系如图所示。下列说法正确的是

A. 1mol d的氧化物含2mol 化学键
B. 工业上电解c的氧化物冶炼单质c
C. 原子半径:a < b < c < d
D. 简单氢化物的沸点:a < d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述中正确的是
A. l00g 9%的葡萄糖水溶液中氧原子数为0.3 NA
B. 标准状况下,2.24L F2通入足量饱和食盐水中可置换出0.1NA个Cl2
C. 工业合成氨每断裂NA个N≡N键,同时断裂6NA个N-H键,则反应达到平衡
D. 常温下l LpH=7的1mol/LCH3COONH4溶液中CH3COO-与NH4+数目均为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年,一些药物引起的不良反应引起了人们的关注。因此在开发新药时如何减少毒副作用是一个很重要的课题。在下列结构简式中,Ⅰ是扑热息痛,Ⅱ是阿司匹林,它们都是临床应用广泛的解热镇痛药,但Ⅰ易导致肾脏中毒,Ⅱ对胃黏膜有刺激性,多用会引起胃溃疡。Ⅲ是扑炎痛,它是根据药物合成中“拼合原理”的方法,设计并合成出的解热镇痛药。这三种物质的结构简式如下:

试回答:
(1)为什么阿司匹林会有上述的毒副作用?___________
(2)合成扑炎痛的反应属于有机化学中的哪一类反应?_________
(3)扑炎痛本身并无解热镇痛的功效,但口服进入人体内后会产生上述药理作用,且毒副作用没有Ⅰ和Ⅱ那么明显,试加以解_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中进行反应:2SO2 (g)+O2(g)![]() 2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )

A. 图Ⅰ表示温度对化学平衡的影响,且甲的温度较高
B. 图Ⅱ表示t0时刻使用催化剂对反应速率的影响
C. 图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响
D. 图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若反应:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ΔH<0在恒温、恒容的密闭体系中进行,下列示意图正确且能说明该反应在进行到t1时刻达到平衡状态的是( )
2CO2(g)+N2(g) ΔH<0在恒温、恒容的密闭体系中进行,下列示意图正确且能说明该反应在进行到t1时刻达到平衡状态的是( )
A.  B.
B. 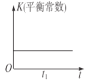 C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为了探究锌与盐酸反应过程中的速率变化,他在100 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(标准状况),实验记录如下(累计值):
时间/min | 1 | 2 | 3 | 4 | 5 |
氢气体积/mL | 50 | 120 | 232 | 290 | 310 |
(1)在0~1 min、1~2 min、2~3 min、3~4 min、4~5 min时间段中,反应速率最大的时间段是________,原因为______________________;反应速率最小的时间段是________,原因为__________________________。
(2)在2~3 min内,用盐酸的浓度变化表示的反应速率为________。
(3)为了减缓反应速率但不减少产生氢气的量,在盐酸中分别加入等体积的下列溶液,其中可行的是________。
A.蒸馏水 B.Na2SO4溶液
C.NaNO3溶液 D.Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知砒霜(As2O3)与锌可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O。
(1)请用“双线桥法”标出电子转移的方向和数目:____________。
(2)砒霜在上述反应中显示出来的性质是_______(填字母)。
A.氧化性 B.还原性 C.酸性 D.碱性
(3)该反应的氧化产物是___,还原产物是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mL0.10 mol/L CuCl2溶液中滴加0.10mol/L Na2S溶液,滴加过程中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示。下列说法正确的是

A. Ksp(CuS)的数量级为10-21
B. 曲线上a点溶液中,c(S2-)c(Cu2+) > Ksp(CuS)
C. a、b、c三点溶液中,n(H+)和n(OH-)的积最小的为b点
D. c点溶液中:c(Na+)>c(Cl-)>c(S2-)>c(OH-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com