
下列物质中,属于非电解质的是
| A.盐酸 | B.NaCl | C.蔗糖 | D.铜 |
科目:高中化学 来源: 题型:单选题
下列表示对应化学反应的离子方程式正确的是
| A.向NaHS溶液中通入Cl2:S2-+Cl2=S↓+2Cl- |
| B.向NaNO2溶液中滴加酸性KMnO4溶液:5NO2-+2MnO4-+3H2O=5NO3-+2Mn2++6OH- |
| C.向NH4HSO4溶液中滴加少量的Ba(OH)2溶液:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+H2O |
| D.向偏铝酸钠溶液中通入过量的CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应的离子方程式正确的是
| A.向稀氨水中加入稀盐酸 OH- + H+ =H2O |
| B.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ |
| C.碳酸钙溶于醋酸中 CaCO3 + 2H+ =Ca2+ + H2O + CO2↑ |
| D.碳酸氢钙溶液跟稀硝酸反应 HCO3-+ H+ = H2O + CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子方程式正确的是
| A.氯化铁溶液中加入铜粉:Fe3++Cu=Fe2++Cu2+ |
| B.等体积、等物质的量浓度的NH4HCO3和Ca(OH)2溶液混合:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| C.水玻璃中通入过量CO2:SiO32-+2CO2+2H2O=H2SiO3(胶体)+2HCO3- |
| D.少量S02通入次氯酸钙溶液中:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应的离子方程式正确的是
A.将氯气溶于水制备次氯酸:Cl2+H2O 2H++Cl-+ClO- 2H++Cl-+ClO- |
| B.少量CO2通入苯酚钠溶液中:2C6H5O-+CO2+H2O=2C6H5OH+CO32- |
| C.Na2O2与H2O混合:2Na2O2+2H2O=4Na++4OH-+O2↑ |
D.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一定能在下列溶液中共存的离子组是( )
| A.加入铝粉有气体放出的溶液中:Na+、NH4+、NO3-、Cl- |
| B.加入NaOH溶液后加热既有气体放出又有沉淀生成的溶液中:Mg2+、NH4+、SO42-、Na+ |
| C.pH=0.3的溶液中:Na+、Al3+、SO42-、CO32- |
| D.存在较多H+、SO42-、NO3-的溶液中:Al3+、CH3COO-、Cl-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
若溶液中由水电离产生的C (OH-)=1×10-14mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是:
| A.Al3+ Na+NO3- Cl- | B.K+ Na+Cl- NO3- |
| C.K+ Na+ Cl-AlO2- | D.K+ NH4+ SO42-NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某无色溶液中含有K+、Cl-、OH-、SO32-、SO42-,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞试液。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。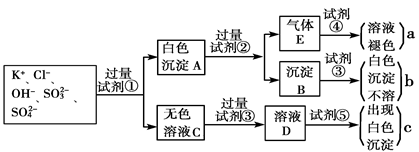
请回答下列问题:
(1)白色沉淀A与试剂②反应的离子方程式是__________________________________。
(2)无色溶液C中加入试剂③的主要目的是____________________________________。
(3)试验中若只加试剂③而不加试剂②,对实验的影响是_______________________。
(4)气体E通入试剂④发生反应的离子方程式是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(17分)铁及其化合物在日常生活、生产中应用广泛。氯化铁和高铁酸钾都是常见的水处理剂。下图为制备氯化铁及进一步氧化制备高铁酸钾的工艺流程。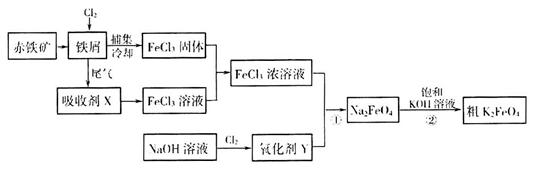
请回答下列问题
(1)已知:①Fe2O3(s)+3C(石墨) 2Fe(s)+3CO(g)△H=+489.0KJ·mol
2Fe(s)+3CO(g)△H=+489.0KJ·mol ;
;
②C(石墨)+CO2(g) 2CO(g)△H=+172.5KJ·mol
2CO(g)△H=+172.5KJ·mol ;用赤铁矿为原料在高炉炼铁过程中发生的主要反应为Fe2O3(s)+3CO(g)
;用赤铁矿为原料在高炉炼铁过程中发生的主要反应为Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)△H= KJ·mol
2Fe(s)+3CO2(g)△H= KJ·mol 。
。
(2)吸收剂x的溶质为____________(写化学式)。
(3)氧化剂Y为“84消毒液”的有效成分,则在碱性条件下反应①的离子方程式为
__________________________________________________________________
(4)过程②是在某低温下进行的,反应的化学方程式为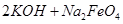 =
=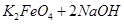 ,说明此温度下
,说明此温度下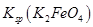 __________
__________ 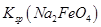 (填“>”或“<”)。
(填“>”或“<”)。
假定此过程中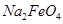 完全转化为
完全转化为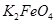 ,若最终制得粗产品
,若最终制得粗产品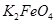 206.25t,产品纯度为96%,则理论上至少需要氧化剂Y的质量是___________t。
206.25t,产品纯度为96%,则理论上至少需要氧化剂Y的质量是___________t。
(5)高铁电池是一种新型二次电池,电解液为强碱溶液,其电池反应为:3Zn+2K2FeO4+8H2O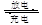 3Zn(OH)2+2Fe(OH)3+4KOH,放电时电池的负极反应式为______________________________________。
3Zn(OH)2+2Fe(OH)3+4KOH,放电时电池的负极反应式为______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com