
【题目】常温下,取![]() HY溶液与
HY溶液与![]()
![]() NaOH溶液等体积混合
NaOH溶液等体积混合![]() 忽略溶液体积的变化
忽略溶液体积的变化![]() ,测得混合溶液的
,测得混合溶液的![]() ,则下列说法正确的是
,则下列说法正确的是![]()
A.混合溶液中由水电离出的![]()
B.溶液中离子浓度由大到小的顺序为![]()
C.![]()
![]()
D.![]()
科目:高中化学 来源: 题型:
【题目】硫酸镁在医疗上具有镇静、抗挛等功效。以菱镁矿(主要成分是MgCO3)为主要原料制备硫酸镁的方法如下:

(1)步骤②中发生反应的离子方程式为____________________________________。
(2)步骤④中调节pH=6.0~6.5的目的是___________________________________。
(3)步骤⑤的操作为______________________________
(4)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH | < 8.0 | 8.0 ~ 9.6 | > 9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为_____[25℃时,Ksp[Mg(OH)2] =5.6×10-12]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海冰是海水冻结而成的咸水冰。海水冻结时,部分来不及流走的盐分以卤汁的形式被包围在冰晶之间,形成“盐泡”![]() 假设盐分以一个NaCl计
假设盐分以一个NaCl计![]() ,其大致结构如下图所示,若海冰的冰龄达到1年以上,融化后的水为淡水。下列叙述正确的是( )
,其大致结构如下图所示,若海冰的冰龄达到1年以上,融化后的水为淡水。下列叙述正确的是( )
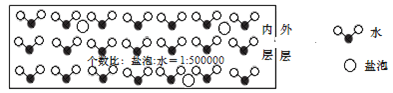
A.海冰内层“盐泡”越多,密度越小
B.海冰冰龄越长,内层的“盐泡”越多
C.海冰内层“盐泡”内的盐分主要以NaCl分子的形式存在
D.海冰内层NaCl的浓度约为![]() 设冰的密度为
设冰的密度为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】单斜硫和正交硫转化为二氧化硫的能量变化图如所示。下列说法正确的是![]()
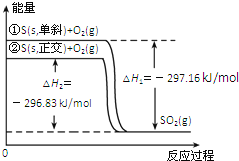
A.![]() ,单斜
,单斜![]() ,正交
,正交![]()
B.正交硫比单斜硫稳定
C.单斜硫燃烧的热化学方程式为:![]() ,单斜
,单斜![]()
D.![]() 式表示断裂1
式表示断裂1 ![]() 中的共价键所吸收的能量比形成1
中的共价键所吸收的能量比形成1 ![]() 中的共价键所放出的能量少
中的共价键所放出的能量少![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程或现象与盐类水解无关的是( )
A. 纯碱溶液去油污 B. 加热氯化铁溶液颜色变深
C. 铁在潮湿的环境中生锈 D. 浓硫化钠溶液有臭味
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化工生产中常用MnS作为沉淀剂除去工业废水中Cu2+:Cu2+(aq)+MnS(s) ![]() CuS(s)+Mn2+(aq),下列说法错误的是( )
CuS(s)+Mn2+(aq),下列说法错误的是( )
A.MnS的Ksp比CuS的Ksp大
B.该反应达平衡时c(Mn2+)=c(Cu2+)
C.往平衡体系中加入少量CuSO4固体后,c(Mn2+)变大
D.该反应的平衡常数K=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.在常温下,下列四种溶液:①0.1mol/L NH4Cl ②0.1mol/L CH3COONH4 ③0.1mol/L NH4HSO4④0.1mol/L NH3H2O,请根据要求填写下列空白:
(1)溶液①呈____ 性(填“酸”、“碱”或“中”),其原因是______(用离子方程式表示)。
(2)在上述四种溶液中,pH最小的是________。
(3)比较四种溶液中c(NH4+)的由大到小的顺序是______________(填序号)。
(4)四种溶液中,离子浓度为0.1 mol/L的是___________(填离子符号)。
Ⅱ. KMnO4溶液常用作氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液很容易被空气中或水中的某些少量还原性物质还原,生成难溶性物质MnO(OH)2,因此配制KMnO4标准溶液的操作如下所述:称取稍多于所需要的KMnO4固体溶于水中,将溶液加热并保持微沸1h;用微孔玻璃漏斗过滤除去难溶的MnO(OH)2;过滤得到的KMnO4溶液贮存于棕色试剂瓶中并放在暗处;利用氧化还原反应滴定法,在70~80℃条件下用基准试剂溶液标定其浓度.
请回答下列问题:
(1)准确量取一定体积的KMnO4溶液需要使用的仪器是_____________。
(2)若选择H2C2O4 2H2O(M=126g/mol)作为基准试剂,准确称取Wg溶于水配成500mL溶液,配制溶液时,所用仪器除烧杯、胶头滴管和玻璃棒外,还需要_______。取25.00mL置于锥形瓶中,用KMnO4溶液滴定至终点,消耗KMnO4溶液VmL,则KMnO4溶液的物质的量浓度为________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关立方烷分子式:C8H8,结构简式![]() ,下列说法不正确的是
,下列说法不正确的是
A.它的一氯代物只有一种同分异构体,其二氯代物有两种同分异构体
B.分子中存在极性键、非极性键,是一种非极性分子
C.它不是芳香烃,但与苯乙烯互为同分异构体
D.它含碳质量分数与乙炔、苯等物质相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2A2(g)+B2(g)![]() 2C(g)ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为wmol·L-1,放出热量bkJ。
2C(g)ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为wmol·L-1,放出热量bkJ。
(1)a________b(填“>”“=”或“<”)。
(2)该反应的平衡常数表达式为________,若将反应温度升高到700 ℃,该反应的平衡常数将________(填“增大”“减小”或“不变”)。
(3)能说明该反应已经达到平衡状态的是________。
a.v(C)=2v(B2) b.容器内压强保持不变 c.v逆(A2)=2v正(B2) d.容器内的密度保持不变
(4)使该反应的反应速率增大,且平衡向正反应方向移动的操作是________。
a.及时分离出C气体 b.适当升高温度 c.增大B2的浓度 d.选择高效的催化剂
(5)密闭容器中,给一氧化碳和水蒸气的气体混合物加热,在催化剂存在下发生反应:CO(g)+H2O(g)![]() H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为________。
H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com