
科目:高中化学 来源: 题型:选择题
| A. | 还原性:Ni>Cu | B. | 氧化性:Cu2+>Ag+ | C. | 还原性:Ag>Cu | D. | 氧化性:Ni2+>Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配位化合物中必定存在配位键 | |
| B. | 配位化合物中只有配位键 | |
| C. | 〔Fe(SCN)6〕3-中的Fe3+提供空轨道,SCN-中的硫原子提供孤电子对形成配位键 | |
| D. | 许多过渡元素的离子(如Cu2+、Ag+等)和某些主族元素的离子或分子(如N3、H+等)都能形成配合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl | B. | NaCl 和 NaBr | C. | NaCl 和 NaI | D. | NaCl 和 I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 装置 | 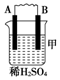 |  |  |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | Cl2有漂白作用 | Cl2能使湿润的有色布条褪色 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | 浓硫酸有强氧化性 | 浓硫酸可用于干燥H2和CO |
| D | 浓氨汽化时要吸收大量的热 | 浓氨可用作制冷剂 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
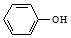 和
和 两种物质的试剂是a(填字母).
两种物质的试剂是a(填字母).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有 CO32- | |
| B. | 某溶液与浓 NaOH 溶液共热,产生使湿润蓝色石蕊试纸变红气体,则原溶液中存在 NH4+ | |
| C. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有 SO 42- | |
| D. | 可用硝酸酸化的 AgNO3 溶液鉴别 Cl-、Br-、I- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com