
| A. | 我们平时应多饮用不二门的水 | |
| B. | 所有天然水都不能饮用 | |
| C. | 人体内含有约$\frac{2}{3}$体重的水,故人每天不用喝水也可 | |
| D. | 人体需要不断补充水分,每人每天需要补充水 |
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某工业废水中含有CN-和Cr2O${\;}_{7}^{2-}$等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理:
某工业废水中含有CN-和Cr2O${\;}_{7}^{2-}$等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | p/400 mol•L-1 | B. | 20 p mol•L-1 | C. | 1.25 p mol•L-1 | D. | 2.5 p mol••L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
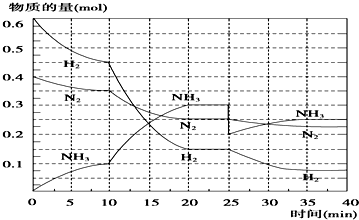
| A | B | C | D | |
| 研究目的 | 压强对反应的影响(P2>P1) | 温度对反应的影响 | 催化剂对反应的影响 | 平衡体系增加N2对反应的影响 |
| 图示 |  |  |  |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸氢钠溶液的pH值小于7 | |
| B. | 久制的氨水pH值变小 | |
| C. | 合成氨工厂通常采用500℃高温,以提高原料的利用率 | |
| D. | 过氧化氢分解加氯化铁溶液作催化剂,使单位时间内产生的氧气的量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | FeCl2、PCl3 | B. | FeCl3、PCl3 | C. | FeCl3、PCl5 | D. | FeCl2、PCl5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com