
| A£® | ¹čµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼£ŗ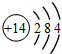 | B£® | ŅŅĻ©·Ö×ӱȥżÄ£ŠĶ£ŗ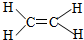 | ||
| C£® | “ĪĀČĖį·Ö×ӵĵē×ÓŹ½£ŗ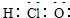 | D£® | ŅŅĖį·Ö×ӵĽį¹¹¼ņŹ½£ŗC2H4O2 |
·ÖĪö A£®¹čŌ×ÓµÄŗĖµēŗÉŹżĪŖ14£¬ŗĖĶāµē×ÓŹżĪŖ14£¬×īĶā²ćĪŖ4øöµē×Ó£»
B£®±ČĄżÄ£ŠĶÖ÷ŅŖĢåĻÖ³öø÷Ō×ÓµÄĻą¶ŌĢå»ż“󊔣¬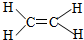 ĪŖ½į¹¹Ź½£»
ĪŖ½į¹¹Ź½£»
C£®“ĪĀČĖįµÄÖŠŠÄŌ×ÓĪŖOŌ×Ó£¬·Ö×ÓÖŠ²»“ęŌŚH-Cl¼ü£»
D£®½į¹¹¼ņŹ½ÖŠÓ¦øƱź³öŗ¬ÓŠ¹ŁÄÜĶŽį¹¹£®
½ā“š ½ā£ŗA£®¹čŌ×ÓµÄŌ×ÓŠņŹż=ŗĖĶāµē×Ó×ÜŹż=14£¬¹čµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ£ŗ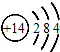 £¬¹ŹAÕżČ·£»
£¬¹ŹAÕżČ·£»
B£®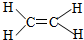 ĪŖŅŅĻ©µÄ½į¹¹Ź½£¬ŅŅĻ©µÄ±ČĄżÄ£ŠĶĪŖ£ŗ
ĪŖŅŅĻ©µÄ½į¹¹Ź½£¬ŅŅĻ©µÄ±ČĄżÄ£ŠĶĪŖ£ŗ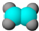 £¬¹ŹB“ķĪó£»
£¬¹ŹB“ķĪó£»
C£®“ĪĀČĖįÖŠŃõŌ×Ó³ÉĮ½øö¹²¼Ū¼ü£¬O-Cl¼üŗĶO-H¼ü£¬“ĪĀČĖįÕżČ·µÄµē×ÓŹ½ĪŖ £¬¹ŹC“ķĪó£»
£¬¹ŹC“ķĪó£»
D£®ŅŅĖį·Ö×ÓÖŠŗ¬ÓŠ¹ŁÄÜĶÅōČ»ł£¬ĘäÕżČ·µÄ½į¹¹¼ņŹ½ĪŖ£ŗCH3COOH£¬¹ŹD“ķĪó£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĮĖ³£¼ū»ÆѧÓĆÓļµÄ±ķŹ¾·½·Ø£¬ĢāÄæÄѶČÖŠµČ£¬Éę¼°±ČĄżÄ£ŠĶ”¢Ō×Ó½į¹¹Ź¾ŅāĶ¼”¢µē×ÓŹ½”¢½į¹¹¼ņŹ½µČÖŖŹ¶£¬Ć÷Č·³£¼ū»ÆѧÓĆÓļµÄŹéŠ“ŌŌņĪŖ½ā“š¹Ų¼ü£¬ŹŌĢāÅąŃųĮĖѧɜµÄ¹ę·¶“šĢāÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | KSCN | B£® | BaCl2 | C£® | HCl | D£® | NaOH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŗĢ¬äå»ÆĒā | B£® | ÕįĢĒ | C£® | ĀĮ | D£® | ĻõĖįČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŠĀÖĘĀČĖ®ÖŠÖ»ŗ¬Cl2ŗĶH2O””·Ö×Ó | |
| B£® | ŠĀÖĘĀČĖ®æÉŹ¹Ą¶É«ŹÆČļŹŌÖ½±äŗģĒŅ²»ĶŹÉ« | |
| C£® | ¹āÕÕĀČĖ®ÓŠĘųÅŻŅŻ³ö£¬øĆĘųĢåŹĒCl2 | |
| D£® | ĀČĖ®·ÅÖĆŹżĢģŗóĖįŠŌ½«±äĒæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaHSO4ČÜŅŗÖŠµĪ¼ÓČėBa£ØOH£©2ČÜŅŗÖĮÖŠŠŌH++Ba2++OH-+SO42-ØTBaSO4”ż+H2O | |
| B£® | ĖįŠŌKMnO4ČÜŅŗÓėĖ«ŃõĖ®·“Ó¦£ŗ2MnO4-+5H2O2+6H+ØT2Mn2++5O2”ü+8H2O | |
| C£® | øÖĢśøÆŹ“Ź±æÉÄÜ·¢ÉśµÄÕż¼«·“Ó¦ĪŖ£ŗ4OH-+4e-ØT2H2O+O2”ü | |
| D£® | ½«ĀČĘųČÜÓŚĖ®Öʱø“ĪĀČĖį£ŗCl2+H2O?2H++Cl-+ClO- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ½«µČĢå»ż”¢µČĪļÖŹµÄĮæÅØ¶ČµÄCH3COONH4ÓėCH3COONaČÜŅŗ»ģŗĻ£ŗc£ØCH3COO-£©£¾c£ØNa+£©£¾c£ØNH4+£©£¾c£ØOH-£© | |
| B£® | ½«µČĢå»ż”¢µČĪļÖŹµÄĮæÅØ¶ČµÄNH4HCO3ÓėNaClČÜŅŗ»ģŗĻ£¬Īö³ö²æ·ÖNaHCO3¾§ĢåŗóµÄČÜŅŗ£ŗc£ØH+£©+c£ØH2CO3£©=c£ØOH-£©+c£ØCO32-£©+c£ØNH3•H2O£© | |
| C£® | Ļņ±„ŗĶĀČĖ®ÖŠ¼ÓČėNaOHČÜŅŗÖĮpH=7£¬ĖłµĆČÜŅŗÖŠ£ŗc£ØNa+£©£¾c£ØClO-£©£¾c£ØCl-£©£¾c£ØOH-£© | |
| D£® | Ļņ0.10mol•L-1 Na2CO3ČÜŅŗÖŠĶØČėÉŁĮæCO2µÄČÜŅŗÖŠ£ŗc£ØOH-£©=c£ØH+£©+c£ØHCO3-£©+2c£ØH2CO3£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬øı䷓ӦĪļÖŠn£ØSO2£©¶Ō·“Ó¦2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©”÷H£¼0µÄÓ°ĻģČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬øı䷓ӦĪļÖŠn£ØSO2£©¶Ō·“Ó¦2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©”÷H£¼0µÄÓ°ĻģČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ·“Ó¦b”¢cµć¾łĪŖĘ½ŗāµć£¬aµćĪ““ļĘ½ŗāĒŅĻņÕż·“Ó¦·½Ļņ½ųŠŠ | |
| B£® | a”¢b”¢cČżµćµÄĘ½ŗā³£ŹżKb£¾Kc£¾Ka | |
| C£® | ÉĻŹöĶ¼ĻóæÉŅŌµĆ³öSO2µÄŗ¬ĮæŌ½øߵƵ½µÄ»ģŗĻĘųĢåÖŠSO3µÄĢå»ż·ÖŹżŌ½øß | |
| D£® | a”¢b”¢cČżµćÖŠ£¬aµćŹ±SO2µÄ×Ŗ»ÆĀŹ×īøß |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com