
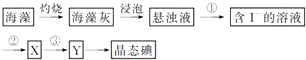

���� ��1������������Һͨ�����ù��˲��������뻥��Һ��ͨ����������ķ�����
��2�����Ȼ�̼��һ����ɫ���ܶȴ���ˮ��Һ�壻F�����õⵥ�������Ȼ�̼���ܽ�ȴ����Ȼ�̼��ˮ�أ��ϲ�Ϊ�Ȼ��أ�
��� �⣺��1���������̿�֪�����벻��������Һ�ķ���Ϊ���ˣ����Դ�����Һ�з������Һ�IJ���Ϊ���ˣ���Ϊ�����л��ܼ��е��ܽ�ȱ�ˮ���ҵ���л��ܼ����ڷ��룬��������ȡ��
�ʴ�Ϊ�����ˣ���ȡ��
��2�����Ȼ�̼��һ����ɫ���ܶȴ���ˮ��Һ�壻���Ȼ�̼������ˮ���ܶȱ�ˮ���ҵⵥ�������Ȼ�̼���ܽ�ȴ���ˮ�У��ڵ��ʵ��ܽ������Ȼ�̼��Ϊ�Ϻ�ɫ���ϲ�Ϊ��Ҫ�������Ȼ��أ�
�ʴ�Ϊ���ޣ����Ϻ죻KCl��
���� ���⿼�������ʵķ�����ᴿ�����չ��ˡ���ȡ������Ȳ����ǽ����Ĺؼ�����Ŀ�ѶȲ�����������������ѧ���ķ�����������������ѧʵ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4��C-H���ij������ | B�� | 4��C-H����ǿ����ͬ | ||
| C�� | 4��C-H���ļн���ͬ | D�� | 4��C-H���ӳ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
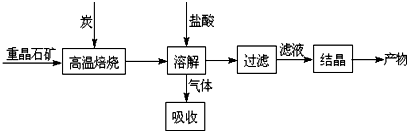
| A�� | ���¶Ȳ��䣬�����������һ������ʱA��Ũ����ԭ����0.48������a+b����c+d | |
| B�� | ����Ӧ��ʼ������ֻ��A��B��ƽ��ʱ��A��B��ת������ȣ���A��B�����ʵ���֮��Ϊ1��1 | |
| C�� | ��ƽ����ϵ�й�������xmol���������г���bmolB���ﵽƽ��ʱ���������ʵ���Ϊ��x+b��mol����a+b=c+d | |
| D�� | ��a+b=c+d�������¶�ʱ��A������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
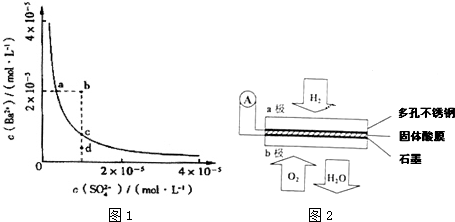
| A�� | ��С���������ƽ�������ƶ� | |
| B�� | ���������ƽ�ⲻ�ƶ������淴Ӧ���ʲ��� | |
| C�� | ����c��X����X��ת�������� | |
| D�� | �����¶ȣ�Y��ת�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʹPH=0����Һ��Fe2+��NO3-��SO42-��I- | |
| B�� | C��H+��=10-14mol•L-1����Һ�У�Na+��AlO2-��S2-��SO32- | |
| C�� | ���Ի����£�Na+��Cu2+��NO3-��SO42- | |
| D�� | ʹ��ɫʯ����Һ������Һ�У�K+��Na+��Ca2+��HCO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ܷ��������ЧӦ�ķ�ɢϵ����Һ | |
| B�� | ��1 L 2 mol/L��FeCl3��Һ�Ƴɽ�������к�����������������Ϊ2NA | |
| C�� | �������ӵĴ�С�뽺�������൱�����������ӵ���ϵ��һ���ǽ��� | |
| D�� | ������FeCl3��Һ���������ڣ��Ƶ�Fe��OH��3���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com