
含C、H、O三种元素的有机物A、B、D,它们的最简式相同。回答下列问题:
(1)在同温同压条件下,同体积的气体A的质量是H2的15倍,1 mol A完全燃烧生成1 mol CO2和1 mol H2O。则A的分子式为________。
(2)有机物B是日常生活中一种调味品的成分。B能和Na2CO3反应放出气体。写出B的同分异构体(能发生银镜反应)的结构简式________________________________________。
(3)有机物D的相对分子质量是A的3倍,D具有酸性,1 mol D与足量Na反应生成22.4 L H2(标准状况)。D在某种催化剂的存在下进行氧化,产物J不发生银镜反应。在浓硫酸存在下,D可发生下列反应:

①写出D中官能团的名称:____________________________________________;
②写出J结构简式:__________________________________________________;
③E→H的化学方程式:________________________________________________
_____________________________________________________________________;
④D→F的化学方程式:_________________________________________________
______________________________________________________________________;
⑤D→G的化学方程式:_________________________________________________
______________________________________________________________________。
科目:高中化学 来源: 题型:
用如图所示的装置进行实验,反应一段时间后断开K,向右侧烧杯中加入0.1 mol
CuO后CuSO4溶液恰好恢复到反应前的浓度和pH。下列说法中不正确的是( )
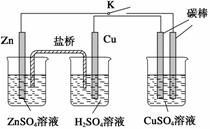
A.铜棒为正极,其电极反应式为2H++2e-===H2↑
B.烧杯右侧碳棒为阴极,其电极表面有红色物质析出
C.反应中消耗锌的质量为13 g
D.导线中通过的电子的物质的量为0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
电子层数相同的短周期元素X、Y、Z、W,其中X的最外层电子数比K层少1个,Y的最外层电子数比K层多1个,Z的单质常用于制造太阳能电池,W的原子半径 是同周期主族元素中最小的。下列推断中正确的是( )
是同周期主族元素中最小的。下列推断中正确的是( )
A.Z的简单氢化物的热稳定性强于W的简单氢化物
B.Z的氧化物与水反应可制得相应的含氧酸
C.X、Y、W的原子半径依次减小,对应的简单离子半径依次增大
D.X、Y、W的最高价氧化物对应的水化物之间互相都能发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项表述,正确的是( )
A. 互为同系物
B.2,2,4,4四甲基己烷若由炔烃加氢而来,则该炔烃为2,2,4,4四甲基1己炔
C.当降冰片烷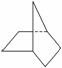 发生一氯取代时,能生成3种沸点不同的产物
发生一氯取代时,能生成3种沸点不同的产物
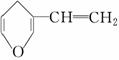 |
D.与 互为同分异构体的芳香族化合物有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物A由C、H、O三种元素组成,相对分子质量为90。将9.0 g A完全燃烧的产物依次通过足量的浓硫酸和碱石灰,分别增重5.4 g和13.2 g。A能与NaHCO3溶液发生反应,且2分子A之间脱水可生成六元环化合物。有关A的说法正确的是( )
A.分子式是C3H8O3
B.A催化氧化的产物能发生银镜反应
 C.0.1 mol A与足量Na反应产生2.24 L H2(标准状况)
C.0.1 mol A与足量Na反应产生2.24 L H2(标准状况)
D.A在一定条件下发生缩聚反应的产物是
查看答案和解析>>
科目:高中化学 来源: 题型:
现有一瓶物质甲和乙的混合物,已知甲和乙的某些性质如下:
| 物质 | 分子式 | 熔点/℃ | 沸点/℃ | 密度/(g/cm3) | 水中溶解性 |
| 甲 | C3H6O2 | -98 | 57.5 | 0.93 | 可溶 |
| 乙 | C4H8O2 | -84 | 77 | 0.90 | 可溶 |
据此,将甲和乙互相分离的最佳方法是( )
A.萃取法 B.升华法 C.蒸馏法 D.分液法
查看答案和解析>>
科目:高中化学 来源: 题型:
“烂版液”是制印刷锌版时,用稀硝酸腐蚀锌版后得到的“废液”(含有少量的Cl-、Fe3+)。某化学兴趣小组拟用“烂版液”制取Zn(NO3)2·6H2O的过程如下:
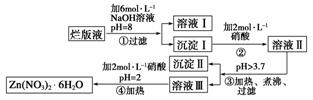
已知:Zn(NO3)2·6H2O是一种无色晶体,水溶液呈酸性,Zn(NO3)2能与碱反应,得到的产物具有两性。
(1)“烂版液”中溶质的主要成分是______(填化学式,下同)。
(2)在操作①中保持pH=8的目的是__________________________________________。
(3)沉淀Ⅰ的主要成分是____________。
(4)操作③中加热煮沸的目的是________________;此步操作的理论依据是
________________________________________________________________________。
(5)操作④保持pH=2的目的是____________;此步操作中所用的主要仪器是
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
(1)氨的水溶液显弱碱性,其原因为 (用离子方程式表示),0.1 mol·L-1的氨水中加入少量的NH4Cl固体,溶液的PH (填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度 (填“增大”或“减小”)。
 (2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为 ,平衡常数表达式为 ;若有1mol硝酸铵完全分解,转移的电子数为 mol。
(2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为 ,平衡常数表达式为 ;若有1mol硝酸铵完全分解,转移的电子数为 mol。
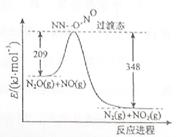
(3)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1molN2, 其△H= kJ·mol-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com