
工业废水中常含有一定量的Cr2O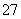 和CrO
和CrO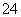 ,它们会对生态系统造成很大的损害,其中还原沉淀法是常用的一种处理方法。流程如下:
,它们会对生态系统造成很大的损害,其中还原沉淀法是常用的一种处理方法。流程如下:
CrO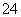
 Cr2O
Cr2O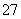
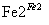 Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓
其中第①步中存在平衡:2CrO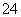 (黄色)+2H+
(黄色)+2H+ Cr2O
Cr2O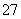 (橙色)+H2O。下列有关说法正确的是
(橙色)+H2O。下列有关说法正确的是
A、第①步当2v(Cr2O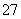 )=v(CrO
)=v(CrO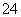 )时,达到了平衡状态
)时,达到了平衡状态
B、对于上述平衡,加入适量稀硫酸后,溶液颜色变黄色,则有利于CrO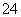 的生成
的生成
C、常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至9
D、第②步中,还原0.1 mol Cr2O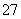 需要91.2 g FeSO4
需要91.2 g FeSO4
【知识点】氧化还原反应 化学平衡 沉淀溶解平衡B3 G2 H5
【答案解析】D解析:没有说明v(Cr2O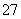 )、v(CrO
)、v(CrO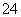 )表示的方向,所以无法判断是否平衡,A错误;加酸后,平衡正向移动,颜色将会变成橙色,有利于Cr2O72-的生成,B错误;c(Cr3+)c3(OH-)= 10-32,c(OH-)=10-9,c(H+)=105,溶液的pH应调至5,C错误;还原0.1 mol Cr2O
)表示的方向,所以无法判断是否平衡,A错误;加酸后,平衡正向移动,颜色将会变成橙色,有利于Cr2O72-的生成,B错误;c(Cr3+)c3(OH-)= 10-32,c(OH-)=10-9,c(H+)=105,溶液的pH应调至5,C错误;还原0.1 mol Cr2O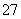 ,则FeSO4失去电子:0.1×2×(6-3)=0.6mol,需要0.6 mol FeSO4,所以需要91.2 g FeSO4,D正确。
,则FeSO4失去电子:0.1×2×(6-3)=0.6mol,需要0.6 mol FeSO4,所以需要91.2 g FeSO4,D正确。
【思路点拨】平衡状态中的v(正)=v(逆)指同种物质的正向速率与逆向速率相等。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
核磁共振(NMR)是研究有机物结构的有力手段之一,在所研究的化合物分子中,每一个结构中的等性氢原子的1H—NMR谱中都给出了相应的峰(信号),谱中峰的强度与结构中的等性氢原子数成正比。现有某种有机物,通过元素分析得到的数据为C∶85.71%,H∶14.29%(质量分数),质谱数据表明它的相对分子质量为84。
(1)该化合物的分子式为____________。
(2)已知该物质可能存在多种结构,A、B、C是其中的三种,请根据下列要求填空:
①A是链状化合物与氢气加成产物分子中有三个甲基,则A的可能结构有________种(不考虑立体异构)。
②B是链状化合物,1H—NMR谱中只有一个信号,则B的结构简式为______________。
③C是环状化合物,1H—NMR谱中也只有一个信号,则C的结构简式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列有机物的结构简式,若有违反系统命名者请予以纠正。
(1)3,5二甲基己烷
____________________,正确名称:____________;
(2)3,3,4,4四甲基2乙基戊烷
____________________,正确名称:____________;
(3)4,4,5,5四甲基3丙基己烷
____________________,正确名称:____________;
(4)2,3,4,5四甲基3乙基5丙基庚烷
____________________,正确名称:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)电镀是将镀件与电源的 极连接。
(2)化学镀的原理是利用化学反应生成金属单质沉淀在镀件表面形成的镀层。
①若用铜盐进行化学镀铜,应选用 (填“氧化剂”或“还原剂”)与之反应。
②某化学镀铜的反应速率随镀液pH变化如右图所示。该镀铜过程中,镀液pH控制在12.5左右。据图中信息,给出使反应停止的方法: 。
(3)酸浸法制取硫酸铜的流程示意图如下:
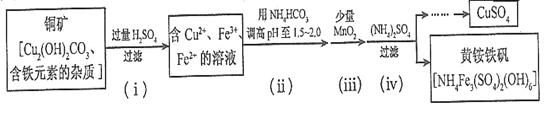
①步骤(i)中Cu2(OH)2CO3发生反应的化学方程式为 。
②步骤(ii)所加试剂起调节pH作用的离子是 (填离子符号)。
③在步骤(iii)发生的反应中,1molMnO2转移2 mol电子,该反应的离子方程式为:
。
④步骤(iv)除去杂质的化学方程式可表示为
3Fe3++NH4++2SO42-+6H2O=NH4Fe3(SO4)2(OH)6↓+6H+,过滤后母液的pH=2.0,
c(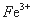 )=a mol·L—1,c(
)=a mol·L—1,c(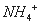 )=b mol·L—1,c(
)=b mol·L—1,c(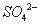 )=d mol·L—1,
)=d mol·L—1,
该反应的平衡常数K= (用含a、b、d的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:HNCO(异氰酸,其结构是H-N=C=O)能和NO2反应生成N2、CO2和H2O。下列有关上述反应的叙述不正确的是
A. HNCO中的氮元素被氧化 B. NO2中的氮元素被还原
C.每生成1mol H2O转移6mol电子 D. CO2是氧化产物
查看答案和解析>>
科目:高中化学 来源: 题型:
将35.8 g Al、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生6.72L气体(标准状况)。另取等质量的该合金溶于过量的稀硝酸中,生成13.44 LNO(标准状况),向反应后的溶液中加入足量的NaOH溶液,得到沉淀的质量为
A. 66.4 g B.50.8 g C 44.8g D. 39.2 g
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g,则下列有关叙述中正确的是
A.加入合金的质量可能为9.6g
B.沉淀完全时消耗NaOH溶液体积为150mL
C.参加反应的硝酸的物质的量为0.4mol
D.溶解合金时产生NO气体体积0.224L(以标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝,在上述溶液中加入足量的亚硫酸钠溶液,蓝色逐渐消失。下列判断不正确的是( )
A.氧化性:ClO –>I2>SO42– B.漂白粉溶液可使淀粉碘化钾试纸变蓝
C.向氯水中加入亚硫酸钠溶液,氯水褪色 D.次氯酸钠可以与亚硫酸钠共存
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,向20 mL 0.2 mol /L H2A溶液中滴加0.2 mol /L NaOH溶液。有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示。根据图示判断,下列说法正确的是( )
A.当V(NaOH)=20 mL时,溶液中离子浓度大小
关系:c(Na+)>c(HA-)> c(A2-) > c(H+) >c(OH-)
B.等浓度的NaOH溶液与H2A溶液按2:1混合后,
其溶液中水的电离程度比纯水大
C.NaHA溶液中:c(OH—)=c(H+)+c(HA–)+2c(H2A)
D.向上述加入20mLNaOH溶液后所得溶液中再加入水的过程中,pH可能减少
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com