
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下
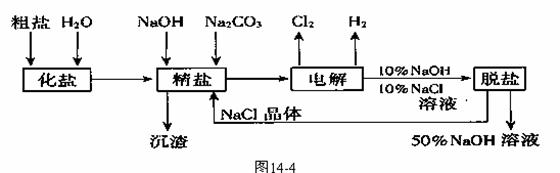
依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为 ,与电源负极相连的电极附近,溶液pH (选填“不变”“升高”或“下降”)。
(2)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是 (选填a,b,c多选扣分)。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(3)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为 (选填a、b、c多选扣分)。
a.先加NaOH,后加Na2CO3,再加钡试剂 b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(4)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为 ___________ 。
科目:高中化学 来源: 题型:
下列有关气体体积的叙述中,正确的是 ( )。
A.在一定的温度和压强下,各种气态物质体积的大小由气体分子的大小决定
B.在一定的温度和压强下,各种气态物质体积的大小由物质的量的多少决定
C.不同的气体,若体积不同,则它们所含的分子数一定不同
D.气体摩尔体积是指1 mol任何气体所占的体积约为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A:4HCl+O2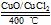 2Cl2+2H2O,可实现氯的循环利用。
2Cl2+2H2O,可实现氯的循环利用。
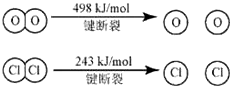 已知:Ⅰ.反应A中,4mol HCl被氧化,放出115.6kJ的热量.
已知:Ⅰ.反应A中,4mol HCl被氧化,放出115.6kJ的热量.
Ⅱ. 则断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为 ( )
A.16kJ B.24kJ C.32kJ D.48kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于能量的变化及反应热的说法中正确的是( )。
A.任何化学反应都有反应热
B.有些化学键断裂时吸收能量,有些化学键断裂时放出能量
C.新化学键的形成不一定放出能量
D.有热量变化的反应一定有化学键的断裂与形成
查看答案和解析>>
科目:高中化学 来源: 题型:
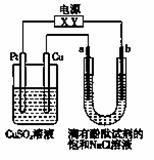
如图,a、b是石墨电极,通电一段时间后,b极附近溶液显红色。下列说法正确的是
A.X极是电源负极,Y极是电源正极
B.a极的电极反应是2Cl--2e-===Cl2↑
C.电解过程中CuSO4溶液的pH逐渐增大
D.Pt极上有6.4 g Cu析出时,b极产生2.24 L(标准状况)气体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关电解质溶液的说法正确的是
A.蒸馏水中逐渐加入NaOH(s)的过程中KW不变
B.CaCO3难溶于稀硫酸,更难溶于醋酸
C.在Na2CO3稀溶液中,c(H+) + c(Na+) = c(OH-) + 2c(CO32—) + c(HCO3-)
D.NaCl溶液和BaCl2溶液中水的KW不同
查看答案和解析>>
科目:高中化学 来源: 题型:
关于下列各实验装置的叙述中,不正确的是( )

① ② ③ ④
A.图①可用于实验室制取少量NH3或O2
B.可用从a处加水的方法检验图②装置的气密性
C.实验室可用图③的方法收集Cl2或NH3
D.利用图④装置制硫酸和氢氧化钠,其中b为阴离子交换膜,c为阳离子交换膜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com