
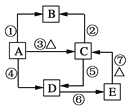
【题目】已知硅及其化合物之间存在如图转化关系。其中A是制造芯片和光电池的主要原料;B是含硅化合物中的一种气体;某些C可作干燥剂或催化剂的载体;D是一种黏合剂,能将磨砂玻璃黏合在一起,E是一种比H2CO3酸性还弱的酸。
试回答下列问题:
(1)写出A、C、E的化学式:A________、C________、E________。
(2)①~⑦反应中,属于氧化还原反应的是____,属于离子反应的是_____。
【答案】 Si SiO2 H2SiO3 ①③④ ④⑤⑥
【解析】
已知硅及其化合物之间存在如图转化关系。其中A是制造芯片和光电池的主要原料,A是硅;B是含硅化合物中的一种气体,B是四氟化硅;某些C可作干燥剂或催化剂的载体,C是二氧化硅;D是一种黏合剂,能将磨砂玻璃黏合在一起,D是硅酸钠,E是一种比H2CO3酸性还弱的酸,E是硅酸。据此解答。
根据以上分析可知A是硅,B是四氟化硅,C是二氧化硅,D是硅酸钠,E是硅酸。则
(1)根据以上分析可知A、C、E的化学式分别是Si、SiO2、H2SiO3。
(2)反应①是硅生成四氟化硅的反应,②是二氧化硅和氢氟酸反应生成四氟化硅和水,③是硅和氧气反应,④是硅和氢氧化钠溶液反应,⑤是二氧化硅和氢氧化钠溶液反应,⑥是硅酸钠转化为硅酸,⑦是硅酸分解生成二氧化硅和水,则①~⑦反应中,属于氧化还原反应的是①③④,属于离子反应的是④⑤⑥。


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
A. 放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B. 充电时阳极反应为:Fe(OH)3-3e-+5OH-=![]() +4H2O
+4H2O
C. 放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,下列说法正确的是

A. 0-t1时,原电池的负极是铜片
B. 0-t1时,正极的电极反应式是2H++2e-=H2↑
C. t1时刻,电流方向发生变化的原因是Al 在浓硝酸中发生钝化,氧化膜阻止了Al进一步反应
D. tl时刻后,电子从铝经过导线流向铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列四组物质的序号按要求填入制定的位置
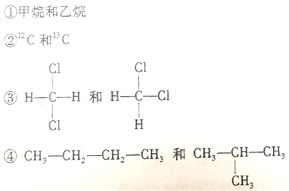
(1)__________组两者互为同位素 (2)_________组两者互为同系物
(3)__________组两者互为同分异构体(4)_________组两者是同一物种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述不正确的是

A. 用图①装置实现铁上镀铜,a 极为铜,电解质溶液可以是CuSO4溶液
B. 图②装置盐桥中 KCl的 Cl-移向乙烧杯
C. 图③装置中钢闸门应与外接电源的负极相连获得保护
D. 图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用两根金属铂做电极,以KOH溶液做电解质溶液,从两极分别通入CH4(g)和O2,则对该燃料电池的下列叙述中正确的是 ( )
A. 负极的电极反应式为:CH4—8e-+10OH-=CO32-+7H2O
B. 负极的电极反应式为:4OH--4e-=2H2O+O2↑
C. 标准状况下,通入5.6 LO2并完全反应后,有2.00mol电子转移
D. 放电一段时间后,通入O2的电极附近溶液的pH降低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com