
 无色孔雀石绿(结构简式如图所示)曾被用作水产养殖业的
无色孔雀石绿(结构简式如图所示)曾被用作水产养殖业的
杀虫剂(鱼药)。因为具有潜在致癌性,已被禁止用作
鱼药。下列关于无色孔雀石绿的叙述中,正确的是
A.分子中所有的碳原子可能在同一平面上
B.无色孔雀石绿属于烃的衍生物
C.无色孔雀石绿可与溴水中的溴发生加成反应
D.在一定条件下,1 mol无色孔雀石绿可以和9 mol氢气发生加成反应
科目:高中化学 来源: 题型:
原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1。a-的电子层结构与氦相同,b和c的次外层有8个电子,c-和d+的电子层结构相同。下列叙述错误的是( )
A.元素的非金属性次序为c>b>a
B.a和其他3种元素均能形成共价化合物
C.d和其他3种元素均能形成离子化合物
D.元素a 、b、c各自最高和最低化合价的代数和分别为0、4、6
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,a、b是石墨电极,通电一段时间后,b极附近溶液显红色。下列说法正确的是( )
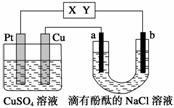
A.X极是电源的负极,Y极是电源的正极
B.Cu电极上增重6.4 g时,b极产生4.48 L(标准状况)气体
C.电解过程中CuSO4溶液的pH逐渐增大
D.a极的电极反应式为2Cl--2e-===Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列排列顺序不正确的是
A.热稳定性:H2O>HF>H2S B.原子半径:Na>Mg>O
C.酸性:HClO4>H2SO4>H3PO4 D.非金属性:F>Cl>Br
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下在一容积恒为2L的容器内发生反应:2A(g) + B(g)  2C(g) ,已知起始投入4mol A(g) 和2mol B(g),经2s后测得C的浓度为0.6 mol/ L,并且2s后各组分浓度不再改变。下列说法正确的是
2C(g) ,已知起始投入4mol A(g) 和2mol B(g),经2s后测得C的浓度为0.6 mol/ L,并且2s后各组分浓度不再改变。下列说法正确的是
A.2s内用物质A表示的平均反应速率为0.3 mol/(L·s)
B.2s内用物质B表示的平均反应速率为0.6 mol/(L·s)
C.2s后每有0.6mol的物质B生成,同时就有0.6mol物质C生成
D.2s时物质B的浓度为0.7mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示为某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。图中A试管盛有无水乙醇(沸点为78℃),B处为螺旋状的细铜丝,C处为无水硫酸铜粉末,干燥管D中盛有碱石灰,E为新制的氢氧化铜,F为氧气的发生装置。

(1)在实验过程中,需要加热的仪器(或区域)有(填仪器或区域的代号A~F)___(4分)。
(2)B处发生的化学反应方程式为________________________________________(2分)。
(3)C处应出现的现象是_________________________________________________(2分),
D处使用碱石灰的作用是_____________________________________________(2分),
E处应出现的实验现象是 ____________________________________________(2分),
F处可以添加的固体药品是 __________________________________________(2分)。
(4)若本实验中拿去F装置(包括其上附的单孔塞和导管),同时将A试管处原来的双孔塞换成单孔塞用以保证装置的气密性,其它操作不变,则发现C处无明显变化,而E处除了依然有上述(3)中所出现的现象之外,还有气体不断地逸出。由此推断此时B处发生反应的化学方程式为___________________________________________________(2分)。
查看答案和解析>>
科目:高中化学 来源: 题型:
元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。下列推测不正确的是( )
A.同周期元素中X的金属性最强
B.原子半径X>Y,离子半径X+>Z2-
C.同族元素中Z的氢化物稳定性最高
D.同周期元素中Y的最高价含氧酸的酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能获得成功的是( )
A.无水乙酸和乙醇共热制取乙酸乙酯
B.将苯逐滴滴入浓硝酸和稀硫酸的混合液中,并用沸水浴加热制取硝基苯
C.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复原来的红色
D.淀粉用酸催化水解后的溶液加入新制银氨溶液,水浴加热,可看到有银镜出现
查看答案和解析>>
科目:高中化学 来源: 题型:
用实验确定某酸HA是弱电解质。两同学的方案是:
甲:①称取一定质量的HA配制0.1 mol·L-1的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;
②分别取这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是________________。
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH______1(填“>”、“<”或“=”)。
乙方案中,说明HA是弱电解质的现象是____________(多选扣分)。
①装HCl溶液的试管中放出H2的速率快;
②装HA溶液的试管中放出H2的速率快;
③两个试管中产生气体的速率一样快。
(3)请你评价:乙方案中难以实现之处和不妥之处:
________________________________________________________________________、
________________________________________________________________________。
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述:________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com