
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和丁的原子核外均有两个未成对电子,乙、丙、丁最高价氧化物对应的水化物两两之间能相互反应。下列说法错误的是( )
A.元素丙的单质可用于冶炼金属 B.甲与丁形成的分子中由非极性分子
C.简单离子半径:丁 > 乙 > 丙 D.甲与乙形成的化合物均有氧化性
【答案】D
【解析】短周期元素甲、乙、丙、丁的原子序数依次增大,甲和丁的原子核外均有两个未成对电子,则甲的核外电子排布是1s22s22p2,甲是C元素,丁的核外电子排布可能是1s22s22p63s23p2,或1s22s22p63s23p4,由于乙、丙、丁最高价氧化物对应的水化物两两之间能相互 反应则丁是核外电子排布的1s22s22p63s23p4,是S元素,丙是Al元素,甲是Na元素。A.由于Al元素的金属活动性较强,一般的还原剂不能把其从化合物中置换出来,要用电解熔融的Al2O3的方法冶炼,正确。B.C与S元素形成的化合物CS2中的化学键是极性共价键,由于两个S原子在C原子的两侧,键角180°,所以形成的分子是非极性分子,正确。D.C形成的化合物CO有强的还原性,CO2有弱的氧化性; Na形成的化合物Na2O2有强的氧化
反应则丁是核外电子排布的1s22s22p63s23p4,是S元素,丙是Al元素,甲是Na元素。A.由于Al元素的金属活动性较强,一般的还原剂不能把其从化合物中置换出来,要用电解熔融的Al2O3的方法冶炼,正确。B.C与S元素形成的化合物CS2中的化学键是极性共价键,由于两个S原子在C原子的两侧,键角180°,所以形成的分子是非极性分子,正确。D.C形成的化合物CO有强的还原性,CO2有弱的氧化性; Na形成的化合物Na2O2有强的氧化 性,而Na2O则氧化性很弱,错误。
性,而Na2O则氧化性很弱,错误。
【考点定位】考查元素周期表、元素周期律的应用的知识。
【名师点睛】元素周期表是学习化学的工具,元素周期律是化学学习的重要规律。利用元素周期表、元素周期律,结合元素的位、构、性三者的密切关系进行元素推断是化学重要的知识。元素原子的核外电子层数是元素在周期表的周期数,最外层电子数是元素原子所在的主族序数,同一周期随着元素原子序数的增大,原子半径逐渐减小,元素的金属性逐渐减弱,非金属性逐渐增强;同一主族的元素从上到下,原子半径逐渐增大,元素的金属性逐渐增强,非金属性逐渐减弱。电子层结构相同的离子核电荷数越大,原子序数越大,离子半径越小,电子层结构不同的离子,离子核外电子层数越多,离子半径就越大。金属的冶炼方 法与金属活动性强弱有关,要掌握金属活动性及冶炼方法,结合物质的性质进行判断,确定其正确性。
法与金属活动性强弱有关,要掌握金属活动性及冶炼方法,结合物质的性质进行判断,确定其正确性。


科目:高中化学 来源: 题型:
m mol乙炔跟n mol氢气在密闭容器中反应,当其达到平衡时,生成p mol乙烯,将平衡混合气体完全燃烧生成CO2和H2O,所需氧气的物质的量是( )
A.(3m+n)mol B.(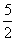 m+
m+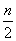 -3p)mol C.(3m+n+2p)mol D.(
-3p)mol C.(3m+n+2p)mol D.( 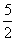 m+
m+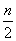 )mol
)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
根据热化学方程式:S(l)+O2(g)===SO2(g) ΔH=-293.23 kJ·mol-1 ,分析下列说法中正确的是( )
A.S(s)+O2(g)===SO2(g),反应放出的热量大于293.23 kJ·mol-1
B.S(g)+O2(g)===SO2(g),反应放出的热量小于293.23 kJ·mol-1
C.1 mol SO2(g)的键能的总和大于1 mol S(l)和1 mol O2(g)的键能之和
D.1 mol SO2(g)的键能的总和小于1 mol S(l)和1 mol O2(g)的键能之和
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知YW的原子充数之和是Z的3倍,下列说法正确的是( )
| Y | Z | ||
| X | W |
A.原子半径:X<Y<Z
B.气态氢化物的稳定性:X>Z
C.Z、W均可与Mg形成离子化合物
D.最高价氧化物对应水化物的酸性:Y>W
查看答案和解析>>
科目:高中化学 来源: 题型:
中国科学技术名词审定委员会已确定第116号元素Lv的名称为鉝。关于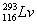 的叙述错误的是( )
的叙述错误的是( )
A.原子序数116 B.中子数177
C.核外电子数116 D.相对原子质量293
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有机物的命名正确的是( )
A. CH3CH2CHOH :2-甲基-1-丙醇
B. CH2BrCH2Br :1,1-二溴乙烷
C. (CH3)2C=CH2 :2-甲基丙烯
D. CH3COOCH2CH2OOCCH3 :乙二酸乙二酯
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的结构简式为 :
它可能发生的反应类型有:①取代 ②加成 ③消去 ④水解 ⑤酯化 ⑥中和 ⑦氧化 ⑧加聚 ( )
A.①②③⑥⑧ B.②③④⑤⑧
C.①②③⑤⑥⑦ D.③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图所示的装置进行实验,反应一段时间后断开K,向右侧烧杯中加入0.1 mol
CuO后CuSO4溶液恰好恢复到反应前的浓度和pH。下列说法中不正确的是( )
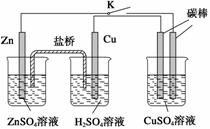
A.铜棒为正极,其电极反应式为2H++2e-===H2↑
B.烧杯右侧碳棒为阴极,其电极表面有红色物质析出
C.反应中消耗锌的质量为13 g
D.导线中通过的电子的物质的量为0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
电子层数相同的短周期元素X、Y、Z、W,其中X的最外层电子数比K层少1个,Y的最外层电子数比K层多1个,Z的单质常用于制造太阳能电池,W的原子半径 是同周期主族元素中最小的。下列推断中正确的是( )
是同周期主族元素中最小的。下列推断中正确的是( )
A.Z的简单氢化物的热稳定性强于W的简单氢化物
B.Z的氧化物与水反应可制得相应的含氧酸
C.X、Y、W的原子半径依次减小,对应的简单离子半径依次增大
D.X、Y、W的最高价氧化物对应的水化物之间互相都能发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com