

科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

 ,
, 
 (3)从环境保护的角度考虑,你
(3)从环境保护的角度考虑,你 认为该实验的设计该如何改进?请写出一种改进方法:
认为该实验的设计该如何改进?请写出一种改进方法:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.不需外加试剂即可鉴别 | B.必须外加试剂才能鉴别 |
| C.如有碘水即能全部鉴别 | D.另有一种溶液即可鉴别 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
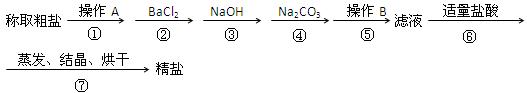
 精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
精盐的实验方案,步骤如下(用于沉淀的试剂稍过量): (5)为检验精盐纯度,需配制150 mL 0.2 mol/L NaCl(精盐)溶液,右图是该
(5)为检验精盐纯度,需配制150 mL 0.2 mol/L NaCl(精盐)溶液,右图是该查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.苯 乙酸乙酯 乙醇 | B.AgNO3 KNO3 Na2CO3 |
| C.MnO2 CuO FeO | D.(NH4)2SO4 K2SO4 NH4Cl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.乙醇中的乙酸(碱石灰,蒸馏) |
| B.乙烷中的乙烯(NaOH溶液,洗气) |
| C.溴苯中的溴(KI溶液,分液) |
| D.乙酸乙酯中的乙酸(饱和NaOH溶液,过滤) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.苯(甲苯):加酸性KMnO4溶液,振荡后分液 |
| B.甲烷(乙烯):通过盛有溴水的洗气瓶 |
| C.乙醇(丙三醇):用分液漏斗分液 |
| D.苯(苯酚):加浓溴水,后过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 aCl溶液(NaHCO3):试剂 ,离子方程式 ;
aCl溶液(NaHCO3):试剂 ,离子方程式 ;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com