
 用Cl2生产某些含氯有机物时会产生副产物HCl.利用反应A,可实现氯的循环利用.反应A:4HCl+O2$\frac{\underline{\;CuO/CuCl_{2}\;}}{400℃}$Cl2+H2O,已知:反应A中,4mol HCl被氧化,放出115.6kJ的热量.
用Cl2生产某些含氯有机物时会产生副产物HCl.利用反应A,可实现氯的循环利用.反应A:4HCl+O2$\frac{\underline{\;CuO/CuCl_{2}\;}}{400℃}$Cl2+H2O,已知:反应A中,4mol HCl被氧化,放出115.6kJ的热量. .
.分析 (1)水是共价化合物,由O原子和2个H原子形成两条共价键;
(2)依据反应A中,4mol HCl被氧化,放出115.6kJ的热量,焓变=反应物断键吸收热量-生成物形成化学键放出热量计算.
解答 解:(1)水是共价化合物,由O原子和2个H原子形成两条共价键,故电子式为 ,故答案为:
,故答案为: ;
;
(2)焓变=反应物断键吸收热量-生成物形成化学键放出热量,4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol,
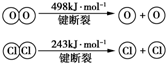
4×E(H-Cl)+498-[243×2+4×E(H-O)]=-115.6,得到4×E(H-O)-4×E(H-Cl)=498-486+115.6=127.6
E(H-O)-E(H-Cl)=31.9≈32,H2O中H-O键比HCl中H-Cl键强,
故答案为:32;强.
点评 本题考查了电子式的书写和化学键键能和焓变关系计算,图象分析判断,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 它们的原子核外电子层数随核电荷数的增加而增多 | |
| B. | 被其他卤素单质从其卤化物中置换出来的可能性随核电荷数的增加而增大 | |
| C. | 它们的氢化物的稳定性随核电荷数的增加而增强 | |
| D. | 单质的颜色随荷电荷数的增加而加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同浓度、同体积的强酸与强碱溶液混合后,溶液的 pH=7 | |
| B. | 0.1 mol•L-1 NH4Cl 溶液与 0.1 mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| C. | 0.1 mol AgCl 和 0.1 mol AgI 混合后加入水中,所得溶液 c(Cl-)=c(I-) | |
| D. | 向 0.10 mol•L-1 Na2SO3溶液中通 SO2气体至溶液 pH=7:c(Na+)<2[c(SO23-)+c(HSO3-)+c(H2SO3)] |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-38 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 结晶牛胰岛素 | B. | 氰酸铵 | C. | 葡萄糖 | D. | 尿素 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验内容 | 实验现象 | 有关反应的方程式或结论 |
| ①取磨光后镁条与铝条,分别投入稀盐酸中 | Mg+2HCl=MgCl2+H2↓ 2Al+6HCl=2AlCl3+3H2↓ 说明金属性的强弱顺序为:Mg>Al | |
| ②向MgCl2、AlCl3溶液中分别逐滴滴入NaOH溶液至过量 | 与MgCl2溶液反应产生白色沉淀,与AlCl3溶液反应先产生白色沉淀,而后沉淀完全溶解 | AlCl3溶液与NaOH溶液反应的化学方程式:AlCl3+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3+NaOH=NaAlO2+2H2O |
| ③向新制的Na2S溶液中滴入新制的氯水 | 生成淡黄色的沉淀 | 反应的化学方程式为:Na2S+Cl2=S↓+2NaCl |
| ④向各为1mol/L的H2SO4、H3PO4溶液中投入镁条 | 镁与H2SO4反应更剧烈,迅速产生大量无色气体 | 说明非金属性的强弱顺序为:S>P |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com