
【题目】第四周期中的 18 种元素具有重要的用途.
(1)金属钒(V)在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价 电子排布式为 , 第四周期元素的第一电离能随原子序 数的增大,总趋势是逐渐增大的,但 Ga 的第一电离能却明显低于 Zn,原因是 .
(2)已知四溴化锗是电子工业中的一种常用试剂,其熔点为 26.1℃,沸点为 186℃,则 GeBr4 的晶体类型为 , 中心原子的杂化类型为 , 与 SiBr4 相比,沸点较低的物质是 .
(3)第四周期ⅤA~ⅦA 族的元素中,电负性由大到小的顺序为(用元素符号表 示) .
(4)如图 1 所示为二维平面晶体示意图,所表示的化学式为 AX3 的是;图 2 为一个金属铜的晶胞,此晶胞立方体的边长为 a cm,金属铜的 密度为 ρ g/cm3 , 则阿伏伽德罗常数可表示为(用含 a、ρ 的代数式表示).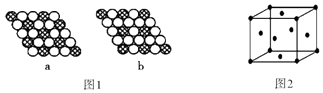
【答案】
(1)3d34s2,Zn原子的价电子排布式为3d104s2,体系的能量较低,原子较稳定,故Zn的第一电离能大于Ga
(2)分子晶体,sp3,SiBr4
(3)Br>Se>As
(4)b,![]()
【解析】解:(1)钒元素的基态原子的简化电子排布式式[Ar]3d34s2,其价电子是排布式为3d34s2,Zn原子的价电子排布式为3d104s2,价电子中3d、4s轨道为全充满状态,原子较稳定,故Zn的第一电离能大于Ga,
所以答案是:3d34s2;Zn原子的价电子排布式为3d104s2,体系的能量较低,原子较稳定,故Zn的第一电离能大于Ga;
(2)四溴化锗的熔沸点低,所以GeBr4是分子晶体;锗与溴形成四个共价键,所以中心原子的杂化类型为sp3,与 SiBr4相比,相对分子质量较小的为SiBr4,所以沸点较低的物质是SiBr4,所以答案是:分子晶体;sp3;SiBr4;
(3)同周期主族元素电负性从左到右渐增,所以第四周期电负性由大到小的顺序:Br>Se>As,
所以答案是:Br>Se>As;
(4)a图中每个斜线球周围有6个白色球,而每个白色球为3个斜线球共有,故斜线球与白色球数目之比=1:6× ![]() =1:2,
=1:2,
b图中每个斜线球周围有6个白色球,而每个白色球为2个斜线球共有,故斜线球与白色球数目之比=1:6× ![]() =1:3,
=1:3,
故图b符合化学式为AX3,
晶胞中含有铜原子数目=8× ![]() +6×
+6× ![]() =4,则晶胞质量为
=4,则晶胞质量为 ![]() g,该晶胞体积为a3 cm3,则
g,该晶胞体积为a3 cm3,则 ![]() g=a3 cm3×ρ g/cm3,故NA=
g=a3 cm3×ρ g/cm3,故NA= ![]() ,
,
所以答案是:b; ![]() .
.


科目:高中化学 来源: 题型:
【题目】图1是元素周期表的一部分.表中所列的字母分别代表一种化学元素. 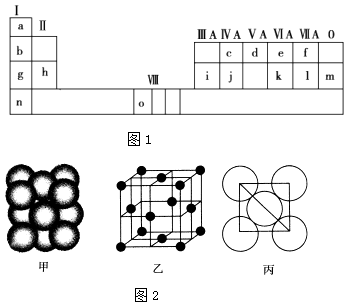
试回答下列问题:
(1)请写出元素o的基态原子外围电子排布式 .
(2)d的氢化物的分子构型为 , 中心原子的杂化形式为;k在空气中燃烧产物的分子构型为 , 中心原子的杂化形式为 , 该分子是(填“极性”或“非极性”)分子.
(3)i单质晶体中原子的堆积方式如图2甲所示,其晶胞特征如图2乙所示,原子之间相互位置关系的平面图如图2丙所示. 若已知i的原子半径为d cm,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
①晶胞中i原子的配位数为 , 一个晶胞中i原子的数目为 .
②该晶体的密度为(用字母表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质互为同分异构体的是( ) ①甲醛和甲醇;②2﹣甲基丁烷和戊烷; ③金刚石和石墨; ④苯甲醇和邻甲苯酚;⑤16O和18O.
A.②③⑤
B.②④
C.③④⑤
D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用酸性含锰废水(主要含Mn2+、Cl﹣、H+、Fe2+、Cu2+)可制备高性能磁性材料(MnCO3)及纯净的氯化铜晶体(CuCl22H2O).工业流程如图: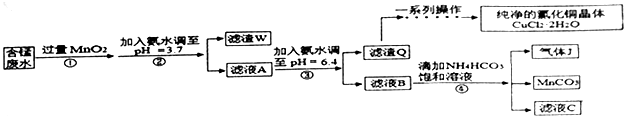
已知:几种金属离子沉淀的pH如表
金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
开始沉淀的pH | 7.5 | 3.2 | 5.2 | 8.8 |
完全沉淀的pH | 9.7 | 3.7 | 6.4 | 10.4 |
回答下列问题:
(1)过程①中,MnO2在酸性条件下可将Fe2+氧化为Fe3+ , 反应的离子方程式为
(2)过程②中,所得滤渣W的成分是 .
(3)过程③中,调pH=6.4目的是 .
(4)过程④中,若生成的气体J可使澄清的石灰水变浑浊,则生成MnCO3反应的离子方程式是 .
(5)将滤渣Q溶解在过量的盐酸中,经过 , 过滤、洗涤、低温烘
(6)过程④中,298K、c(Mn2+)为1.05mol/L时,实验测得MnCO3的产率与溶液pH、反应时间关系如图据图中信息,你选择的最佳pH是;理由是 . 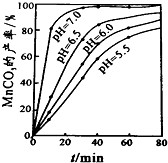
(7)从滤液C可得到的副产品是(填化学式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是( )
A.10 g 46%的乙醇水溶液中所含氢原子数目为1.2NA
B.标准状况下,2.24 L氯气溶于水发生反应,转移的电子数目为0.1NA
C.高温下,0.2 mol的铁与足量的水蒸气反应,生成氢气的分子数目为0.3NA
D.25℃时,100 mL pH=13的Ba(OH)2溶液中OH﹣的数目为0.02NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出.二氧化硒(Se)是一种氧剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se. 完成下列填空:
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2 2NaFeO4+2Na2O+2Na2SO4+O2↑
该反应中的氧化剂是 . 简要说明K2FeO4 , 作为水处理剂时,在水处理过程中所起的作用
.
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、ClO﹣、OH﹣、FeO ![]() 、Cl﹣、H2O.每生成1molFeO
、Cl﹣、H2O.每生成1molFeO ![]() 转移mol电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为mol.
转移mol电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为mol.
(3)已知:
Se+2H2SO4(浓)2SO2↑+SeO2+2H2O
2SO2+SeO2+2H2OSe+2SO42﹣+4H+
SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是 .
(4)回收得到的SeO2的含量,可以通过下面的方法测定:
①SeO2+KI+HNO3Se+I2+KNO3+H2O ②I2+2Na2S2O3Na2S4O6+2NaI
配平方程式①,标出电子转移的方向和数目. .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写不正确的是
A. 盐酸与Na2SiO3溶液混合: SiO32-+2H+=H2SiO3↓
B. 浓盐酸和二氧化锰共热制取Cl2: MnO2+4H++2Cl- ![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
C. NO2通入水中: H2O+3NO2=2H++2NO3-+NO
D. 向澄清石灰水中通人过量SO2: SO2+Ca2++2OH-=CaSO4↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com