
| A、HCO3-+H2O?H2CO3+OH- |
| B、CH3COONa?CH3COO-+Na+ |
| C、Ca(OH)2?Ca2++2OH- |
| D、NH3?H2O?NH4++OH- |


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
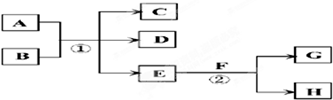
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X2Y3 |
| B、XY3 |
| C、X2Y2 |
| D、X3Y4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L水中所含的分子数约为6.02×1023个 | ||
| B、1 mol Cl2参加反应转移电子数一定为2 NA | ||
C、标准状况下,aL氧气和氮气的混合物含有的分子数约为
| ||
| D、从1 L 0.5 mol/LNaCl溶液中取出100 mL,剩余溶液中NaCl物质的量浓度为0.45mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、直接排放含磷生活污水 |
| B、大量使用氟里昂作为冰箱制冷剂 |
| C、使用可降解塑料代替不可降解塑料 |
| D、使用不易分解的有机氯农药 |
查看答案和解析>>
科目:高中化学 来源: 题型:
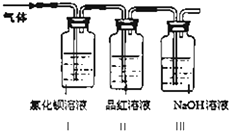
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com