
| A. | Na+、Cu2+、Cl-、CO32- | B. | HCO3-、Cl-、Fe3+、Na+ | ||
| C. | Cl-、K+、NO3-、Fe2+、 | D. | S2-、SO42-、NH4+、Fe2+ |
分析 离子在溶液中可以大量共存,说明离子之间不发生任何反应,加OH-产生沉淀,溶液中可能存在Fe2+、Cu2+、Mg2+离子,加H+生成气体,说明溶液中可能存在CO32-或HCO3-离子或发生其它生成气体的反应,以此解答该题.
解答 解:A.Cu2+与CO32-反应生成沉淀而不能大量共存,故A错误;
B.HCO3-、Fe3+发生互促水解反应而不能大量共存,故B错误;
C.离子之间不发生任何反应,加OH-产生氢氧化亚铁沉淀,加H+发生氧化还原反应生成NO气体,符合题意,故C正确;
D.S2-、Fe2+反应生成沉淀而不能大量共存,故D错误.
故选C.
点评 本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应的离子共存考查,注意与酸、碱的反应,题目难度不大.


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:解答题
 如图为氨气溶于水的喷泉实验装置(图中固定装置均已略去).
如图为氨气溶于水的喷泉实验装置(图中固定装置均已略去).查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
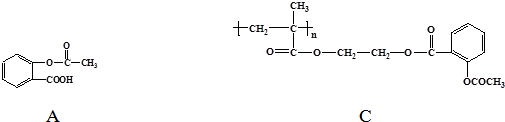
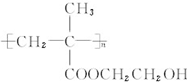 .
.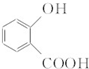 和CH3COOH(写结构简式).
和CH3COOH(写结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A2B6 | B. | A2B3 | C. | A3B | D. | AB3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
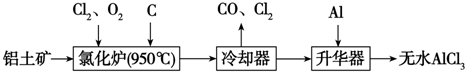
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 操作 | 现象 |
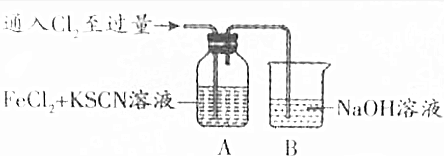 | Ⅰ.装置A中溶液变红 Ⅱ.稍后,溶液由红色变为黄色 |
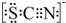
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
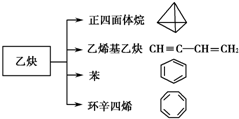 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物. .
. 、
、 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com