
分析 电解质:在水溶液中或熔融状态下能够导电的化合物,
非电解质:在熔融状态下和水溶液中都不能导电的化合物,
单质和混合物既不是电解质也不是非电解质,
解题抓住电解质和非电解质都必须是化合物而不是单质或混合物,以及导电是在水溶液或熔融状态下为条件.同时注意CO2、SO2、SO3、NH3等虽然溶于水能导电,但导电实质是H2CO3、H2SO3、H2SO4、NH3•H2O,不属于电解质,酸碱盐则是电解质.
解答 解:①NaCl溶液是混合物,电解质和非电解质都必须是化合物,选项①既不是电解质也不是非电解质;
②NaOH在水溶液中或熔融状态下能够电离出钠离子和氢氧根离子,能导电,NaOH是化合物,选项②属于电解质;
③H2SO4在水溶液中能电离出氢离子和硫酸根离子,能导电,是化合物,选项③属于电解质;
④Cu是单质,不是化合物,选项④既不是电解质也不是非电解质;
⑤CH3COOH在水溶液中能电离出乙酸根离子和氢离子,能导电,是化合物,选项⑤属于电解质;
⑥CO2的水溶液虽然能导电,但导电的离子是二氧化碳和水反应生成的碳酸电离出的,不是二氧化碳自身电离的,选项⑥属于非电解质;
⑦乙醇在水溶液中以乙醇分子的形式存在,是非电解质,选项⑦属于非电解质;
⑧水是化合物,能电离出氢离子和氢氧根离子,是弱电解质,选项⑧属于电解质;
故答案为:②③⑤⑧;⑥⑦;①④.
点评 本题考查了电解质、非电解质概念的实质分析判断,注意判断的依据应用,掌握基础是解题关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | Na+ClO- K+ NO3- | B. | K+ Na+ NO3- SO32- | ||
| C. | K+ Fe2+ SO42- NO3- | D. | NH4+ Al3+ SO42- NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O中氧元素的化合价为-l | B. | Na2O2中氧元素的化合价为-2 | ||
| C. | NaOH中氧元素的化合价为-1 | D. | Na2O中氧元素的化合价为-2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
| A. | a=1.64 | |
| B. | 此时正反应速率大于逆反应速率 | |
| C. | 若起始时加入2a mol CH3OH,则达到平衡时CH3OH的转化率增大 | |
| D. | 若混合气体的平均摩尔质量不再变化,则说明反应已达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用甘氨酸(H2NCH2COOH)和丙氨酸(CH3CHNH2COOH)缩合,最多可形成4种二肽 | |
| B. | 在酸性条件下,CH3CO18OC2H5水解的产物是CH3CO18OH和C2H5OH | |
| C. | 实验室用如图装置证明酸性:醋酸>碳酸>苯酚,①中放入浓醋酸,②中放入CaCO3,③中放入C6H5ONa溶液 | |
| D. | 实验室用如图装置证明乙炔具有还原性,①中放入H2O,②中放入电石,③中放入KMnO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2和D2互为同素异形体 | B. |  和 和  互为同分异构体 互为同分异构体 | ||
| C. |  和 和  是同一种物质 是同一种物质 | D. | 乙醇的同分异构体是HO-CH2CH2-OH |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 阳离子 | Na+,Ba2+,NH4+ |
| 阴离子 | CH3COO-,Cl-,OH-,SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:推断题
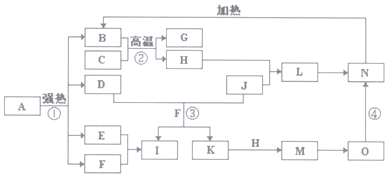
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com