
| A. | 工业上合成氨,及时分离出产物氨有利于提高氮气的转化率 | |
| B. | 实验室中常用排饱和食盐水的方法收集氯气 | |
| C. | 由H2、I2(g)、HI组成的平衡体系,加压后颜色加深 | |
| D. | 工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
分析 勒沙特列原理是如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动.勒沙特列原理适用的对象应存在可逆过程,如与可逆过程无关,则不能用勒沙特列原理解释.
解答 解:A、分离出生成物,平衡向着正向移动,有利于氨气的合成,所以可以勒夏特列原理解释,故A不选;
B、氯化钠在溶液中完全电离,所以饱和食盐水中含有大量的氯离子,氯气溶于水的反应是一个可逆反应,Cl2+H2O?HClO+H++Cl-,由于饱和食盐水中含有大量的氯离子,相当于氯气溶于水的反应中增加了大量的生成物氯离子,根据勒夏特列原理,平衡向逆反应方向移动,氯气溶解量减小,所以可以勒夏特列原理解释,故B不选;
C、氢气和碘反应生成HI的反应前后气体计量数之和不变,压强不影响平衡移动,H2、I2、HI平衡混和气加压后碘浓度增大,所以颜色变深,但平衡不移动,所以不能用平衡移动原理解释,故选C;
D、工业上生产硫酸存在平衡2SO2+O2?2SO3,使用过量的空气,增大氧气的浓度,平衡向正反应移动,可以提高二氧化硫的利用率,能用勒夏特列原理解释,故D不选;
故选C.
点评 本题考查了工业合成氨的反应原理及反应条件的选择,题目难度中等,明确合成原理为解答关键,注意掌握影响化学平衡的因素,试题侧重考查学生的分析、理解能力及灵活应用基础知识的能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 3NO2+H2O═2HNO3+NO | B. | Fe+CuSO4═FeSO4+Cu | ||
| C. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | D. | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 相关信息 | |
| X | 单质为双原子分子.若低温蒸发液态空气,因其沸点较低可先获得X的单质 |
| Y | 含Y元素的物质焰色反应为黄色 |
| Z | 同周期元素中原子半径最小 |
| R | R元素原子的最外层电子数是K层电子数的3倍 |
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(M)=0.3mol/(L•s) | B. | v(N)=0.6mol/(L•s) | C. | v(P)=0.4mol/(L•s) | D. | v(Q)=0.45mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 ;④CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O;
;④CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O; 查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)3COH的名称:2,2二甲基乙醇 | B. | 甲烷的球棍模型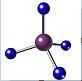 | ||
| C. | 乙醛的结构式:CH3CHO | D. | 四氯化碳分子的电子式: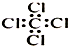 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知反应Cu(s)+2Ag+ (aq)═Cu2+(aq)+2Ag(s)为一自发进行的氧化还原反应,将其设计成如图所示原电池.下列说法中正确的是( )
已知反应Cu(s)+2Ag+ (aq)═Cu2+(aq)+2Ag(s)为一自发进行的氧化还原反应,将其设计成如图所示原电池.下列说法中正确的是( )| A. | 银电极质量逐渐减小,Y溶液中c(Ag+)增大 | |
| B. | 实验过程中取出盐桥,原电池仍继续工作 | |
| C. | 电极X是正极,其电极反应为Cu-2e-═Cu2+ | |
| D. | 当X电极质量减少0.64g时,外电路中有0.02mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 试剂 选项 | 甲组 | 乙组 |
| A | 新制氯水、KSCN溶液 | NaOH溶液 |
| B | 酸性KmnO4溶液 | KSCN溶液 |
| C | KOH溶液 | 溴水 |
| D | 溴水 | 酸性KmnO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com