
| A. | 绿色荧光蛋白分子中氨基酸排列顺序一定相同 | |
| B. | 绿色荧光蛋白能发生颜色反应及盐析、变性等 | |
| C. | 绿色荧光蛋白可发生水解反应生成多种氨基酸 | |
| D. | 绿色荧光蛋白可用于跟踪生物细胞的分子变化 |
科目:高中化学 来源: 题型:实验题

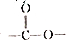 共有6种,其中核磁共振氢谱有3组峰,且锋面积之比为6:1:1的任意一种结构简式为HCOOCH(CH3)2或CH3)2CHCOOH.
共有6种,其中核磁共振氢谱有3组峰,且锋面积之比为6:1:1的任意一种结构简式为HCOOCH(CH3)2或CH3)2CHCOOH.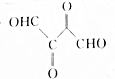 仿照上述题目中工艺图示设计流程为CH2=CHCH=CH2$\stackrel{溴}{→}$CH2BrCHBrCHBrCH2Br$→_{△}^{氢氧化钠溶液}$CH2OHCHOHCHOHCH2OH$→_{铜、△}^{氧气}$
仿照上述题目中工艺图示设计流程为CH2=CHCH=CH2$\stackrel{溴}{→}$CH2BrCHBrCHBrCH2Br$→_{△}^{氢氧化钠溶液}$CH2OHCHOHCHOHCH2OH$→_{铜、△}^{氧气}$ .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g)+3B(g)?2C(g)△H=-192kJ•mol-1.向M、N中,都通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )
如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g)+3B(g)?2C(g)△H=-192kJ•mol-1.向M、N中,都通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )| A. | 平衡时A气体在两容器中体积分数可能相等 | |
| B. | 若x:y=1:2,则平衡时,M中的转化率:A>B | |
| C. | 若x:y=1:3,当M中放出热量172.8 kJ时,A的转化率为90% | |
| D. | 若x=1,y=3,则达到平衡时反应物的转化率N<M |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在稀溶液中,1mol酸和1mol碱完全反应所放出的热量叫做中和热 | |
| B. | 在101kPa时,1mol物质燃烧时的反应热叫做该物质的燃烧热 | |
| C. | 对于热化学方程式S(s)+O2(g)═SO2(g)△H1 S(g)+O2(g)═SO2(g)△H2,化学反应的△H前者大于后者 | |
| D. | 如果反应物所具有的总能量低于生成物所具有的总能量,则发生的反应是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
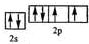 ,该元素的名称是氧;
,该元素的名称是氧;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.06 mol/(L•s) | B. | 1.8mol/(L•s) | C. | 1.2 mol/(L•s) | D. | 0.18 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴苯的制备: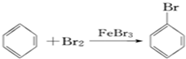 | |
| B. | 1,3-戊二烯发生加聚反应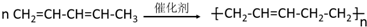 | |
| C. | 苯酚钠溶液中通入少量二氧化碳: | |
| D. | 醇可以制备卤代烃,如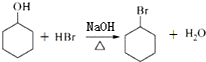 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
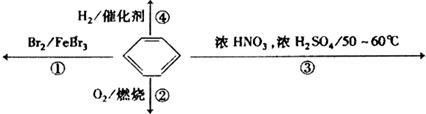
| A. | 反应①为取代反应,有机产物的密度比水小 | |
| B. | 反应③为取代反应,有机产物是一种烃 | |
| C. | 反应④中1mol苯最多与3 mol H2发生加成反应,是因为苯分子含有三个碳碳双键 | |
| D. | 反应②为氧化反应,反应现象是火焰明亮并带有较多的黑烟 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com