
 按要求完成下列小题.
按要求完成下列小题.分析 (1)1mol氨气分子中含有1molN原子、3molH原子,每个NH3分子含有10个质子,故质子物质的量为NH3分子的10倍,根据分子呈电中性,电子的物质的也是分子物质的量的10倍,由此分析解答;
(2)根据n=$\frac{N}{{N}_{A}}$计算出3.01×1023个Cl-的物质的量,再根据化学式MCl2计算出MCl2的物质的量,再根据M=$\frac{m}{n}$计算出M的摩尔质量,摩尔质量在数值上等于其相对原子或分子质量;
(3)①根据c=$\frac{1000ρω}{M}$计算该盐酸的物质的量浓度;
②根据稀释定律,稀释前后溶质的物质的量不变,据此计算需要浓盐酸的体积.
解答 解:(1)0.5molNH3中含有0.5mol氮原子,1.5mol的氢原子,含有质子物质的量=0.5mol×10=5mol,电子的个数为:0.5×10×NA=5NA,故答案为:5NA;
(2)27.75g某+2价金属的氯化物(MCl2)中含有3.01×1023个Cl-,3.01×1023个Cl-的物质的量为:n(Cl-)=$\frac{3.01×1{0}^{23}}{6.02×1{0}^{23}}$mol=0.5mol,MCl2的物质的量为:n(MCl2)=$\frac{1}{2}$×0.5mol=0.25mol,M(MCl2)=$\frac{27.75g}{0.25mol}$=111g/mol,则M的相对原子质量为:111-36.5×2=40,故答案为:40;
(3)①根据c=$\frac{1000ρω}{M}$可知,该盐酸的物质的量浓度为$\frac{1000×1.19×36.5%}{36.5}$mol/L=11.9mol/L;
②根据稀释定律,稀释前后溶质的物质的量不变,需要浓盐酸的体积为$\frac{200mL×1mol/L}{11.9mol/L}$=16.8mL,
故答案为:11.9mol/L;16.8.
点评 本题考查物质的量有关计算,难度不大,注意对公式的理解掌握与灵活应用.


 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案科目:高中化学 来源: 题型:推断题
| 族 周期 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 |
| 2 | ④ | ⑦ | ||||||
| 3 | ① | ② | ③ | ⑤ | ⑥ | ⑧ | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. | 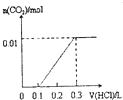 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)/c(OH-)=1012的水溶液中:NH4+、Al3+、NO3- | |
| B. | pH=1的溶液中:Fe2+、NO3-、SO42- | |
| C. | 水电离出的c(H+)=10-12mol/L的溶液中:Ca2+、Cl-、HCO3- | |
| D. | c (Fe3+)=0.1mol/L的溶液中:K+、SO42-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| B. | 40 g NaOH溶解在1 L水中,所制得的溶液,物质的量浓度为1 mol•L-1 | |
| C. | 标准状况下,11.2 L四氯化碳所含分子数为0.5NA | |
| D. | 常温常压下,5.6g铁与过量的盐酸反应转移电子总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 | B. | 3 | C. | 2 | D. | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ②③④ | C. | ①④⑤ | D. | ③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不慎将酸溅到眼中,应立即用氢氧化钠水溶液冲洗,边洗边眨眼睛 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸 | |
| C. | 酒精灯着火时可用水扑灭 | |
| D. | 配制硫酸溶液时,可先在量筒中加入一定量的水,再搅拌条件下慢慢加入浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X 与 Y 只能形成一种化合物 | |
| B. | 单质的氧化性:X<M | |
| C. | 气态氢化物的稳定性:M>N | |
| D. | 最高价氧化物对应水化物的碱性:Y>Z |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com