
【题目】下图为有关分子在催化剂作用下发生转化的示意图,下列叙述正确的是( )。

A.N2→NH3,NH3→NO均属于氮的固定
B.催化剂a作用下氮原子发生了氧化反应
C.催化剂a、b表面均发生了极性共价键的断裂
D.使用催化剂a、b均可以提高单位时间内生成物的产量
 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】合成一种用于合成 γ 分泌调节剂的药物中间体,其合成的关键一步如图。下列有关化合物甲、乙的说法正确的是
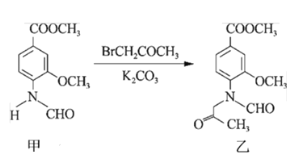
A.甲→乙的反应为加成反应
B.甲分子中至少有 8 个碳原子在同一平面上
C.甲、乙均不能使溴水褪色
D.乙与足量 H2 完全加成的产物分子中含有 4 个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素![]() 在元素周期表中的相对位置如图所示,其中w原子的最外层电子数是最内层电子数的3倍.下列判断不正确的是
在元素周期表中的相对位置如图所示,其中w原子的最外层电子数是最内层电子数的3倍.下列判断不正确的是![]()

A.x与同主族且相邻元素的气态氢化物的沸点,前者高于后者
B.含Y元素的盐溶液有的显酸性,有的显碱性
C.x的气态氢化物与w的最高价氧化物的水化物反应只能生成一种盐
D.x与H、O元素形成的化合物可以组成一种盐,其中![]() 元素原子个数之比为2:4:3
元素原子个数之比为2:4:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基铁[Fe(CO)5]广泛用于催化剂,汽油抗爆剂,电子工业高频线圈制造。请回答下列问题:
(1)羰基铁[Fe(CO)5]中,碳、氧电负性大小比较____(用元素符号表示)。写出基态O的轨道表示式____;
(2)CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO分子中C原子的杂化类型为____杂化。
(3)1molFe(CO)5分子中含σ键数目为____;CO配体中的配位原子是____。
(4)科学家通过X射线探明,FeO、MgO、CaO的晶体结构与NaCl晶体结构相似,比较晶体熔点的高低MgO____CaO(填“高于”或“低于”)
(5)羰基铁[Fe(CO)5]中铁为0价。如图中的羰基铁为+3价,此羰基铁的晶体类型为____;此羰基铁中每个铁的配位数是____。
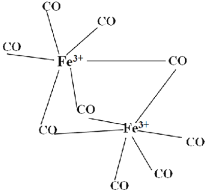
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表中部分元素某种性质![]() 值
值![]() 随原子序数变化的关系。
随原子序数变化的关系。
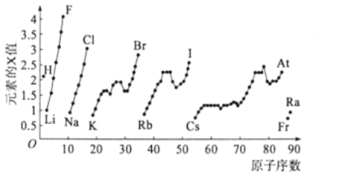
(1)短周期中原子核外p能级上电子总数与s能级上电子总数相等的元素是______![]() 填元素符号
填元素符号![]() 。
。
(2)同周期,随着原子序数的增大,X值变化趋势为______再结合同主族不同元素的X值变化的特点,体现了元素性质的______变化规律。
(3)X值较小的元素集中在元素周期表的______![]() 填序号
填序号![]()
A.左下角![]() 右上角
右上角![]() 分界线附近
分界线附近
(4)下列关于元素此性质的说法中正确的是______![]() 填序号
填序号![]() 。
。
A.X值可反映元素最高正化合价的变化规律
B.X值可反映原子在分子中吸引电子的能力
C.X值的大小可用来衡量元素金属性和非金属性的强弱
(5)SiHCl3与水发生的化学反应可认为是广义的水解反应,根据图中数据,该反应的化学方程式为______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向50mL含有0.1molCl2的氯水中滴加2mol·L1的NaOH溶液,得到溶液pH随加入NaOH溶液体积的变化如图所示。下列说法正确的是
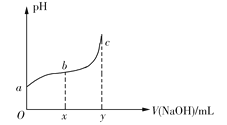
A.若a点pH=4,且c(Cl)=mc(HClO),则HClO的电离平衡常数为![]()
B.若x=100,b点对应溶液中,c(OH)>c(H+),可用pH试纸测定其pH
C.若y=200,c点对应溶液中,c(OH)c(H+)=2c(Cl)+c(HClO)
D.b→c段,随NaOH溶液的滴入,![]() 逐渐增大
逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家成功合成了世界上首个五氮阴离子盐(H3O)3(NH4)4(N5)6Cl(用R代表),请根据其组成的元素和结构回答下列问题:
(1)氮原子价层电子的轨道表达式为_____________________。
(2)第一电离能N______O(填“>”、“<”或“=”),其原因是_____________。
(3)经X射线衍射测得化合物R的晶体结构,其局部结构如下图所示。
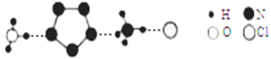
①R中两种阳离子的相同之处为_________,不同之处为__________。(填标号)
a.中心原子的杂化轨道类型 b.中心原子的价层电子对数
c.立体结构 d.共价键类型
②R中阴离子N5-中的σ键总数为________个。大π键可用符号πmn表示,其中m为形成大π键的原子数,n为形成大π键的电子数,则N5-中的大π键应表示为__________。
③图中虚线代表氢键,其表示式为(NH4+)NH…Cl、___________、____________。
(4)提取炼铜的阳极泥中金、银、铂时,用到王水(HNO3和HCl的物质的量之比为1∶3的混酸),过程如下:
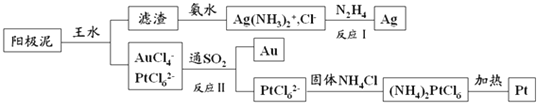
①滤渣的成分是_____________,(NH4)2PtCl6中配体是_______________________。
②金和浓硝酸反应的化学方程式为:Au+6HNO3(浓)=Au(NO3)3+3NO2↑+3H2O,该反应的平衡常数很小,几乎不反应,但金却可以溶于王水,原因是____________________,试写出该反应的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,需要提纯后才能综合利用,粗盐精制的实验流程如下。
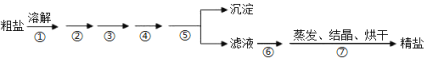
(1)下列说法不正确的是(__________)
A.在第①步中使用玻璃棒搅拌可加速粗盐溶解
B.第⑤步操作是过滤
C.在第②③④⑥步通过加入化学试剂除杂,加入试剂顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→稀盐酸
D.除去MgCl2的离子方程式为:Mg2++2OH=Mg(OH)2↓
(2)判断SO42-已除尽的方法是___。
(3)电解精制NaCl溶液可得到NaOH、Cl2和H2,它们是重要的化工原料。有关反应关系如图所示:(部分反应条件和物质省略)
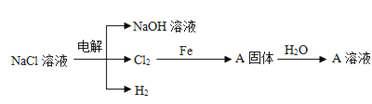
①Cl2与NaOH溶液反应可以制取“84”消毒液,发生反应的离子方程式为:__。
②写出Cl2和铁反应化学方程式,并用双线桥标出电子转移的方向和数目:__,标准状况下,22.4LCl2与足量的Fe反应,则反应过程中转移__个电子。
(4)向足量A溶液中加入少量的钠完全反应前后A溶液质量变化__(填“增大”或“减小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BF3与一定量的水形成(H2O)2·BF3,一定条件下(H2O)2·BF3可发生如图转化,下列说法中正确的是

A.(H2O)2·BF3熔化后得到的物质属于离子晶体
B.(H2O)2·BF3分子间存在着配位键和氢键
C.BF3是仅含极性共价键的非极性分子
D.基态B原子核外电子的空间运动状态有5种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com