
����֮Ϊ������ء���ֽ�ʵ�أ����ñ���ֽƬ��Ϊ�����壬����ܷ�ӦΪ:Zn+2MnO2+ H2O=ZnO+2MnO(OH)�������˴�ͳ�������������Ⱦ���⣬����Ͼɵ�ֽ�ʵ�ؿ���Ϊһ��ķ�������Դ���������˵������ȷ����
A���õ�ط�Ӧ��пԪ�ػ��ϼ�����
B���õ�ط�Ӧ�ж�������������
C���乤��ԭ���ǽ���ѧ��ת��Ϊ����
D���������øõ�ؿ��Լ��ٶԻ�������Ⱦ
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ̩���и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и�����������ԭ�ӵ�������Ӳ���ﵽ8�����ȶ��ṹ���ǣ� ��
A. N2 B. HClO C. CH4 D. BF3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������һ�и�һ����ĩ��ѧ�Ծ��������棩 ���ͣ������
CO2��CS2��COS����C��O��S����Ԫ���γɵĽṹ���ƵĻ����
��1��������˵��̼��������Ԫ�طǽ��������ǿ������ ������ţ�
a����������Һ����Na2CO3��Һ�У���������
b�������ԣ�ŨH2SO4��H2CO3
c��CS2��̼Ԫ��Ϊ+4�ۣ���Ԫ��Ϊ��2��
d��SO2�н�ǿ��ԭ�ԣ���CO2��ԭ��
��2���ʻ���COS������Ϊһ��Ѭ�������ܷ�ֹijЩ���桢�߳��Σ����
���ʻ���ĽṹʽΪ�� ���е㣺CO2_____COS������ڡ���С�ڡ� ����˵��ԭ��________��
�������й��ʻ�����Ʋ�϶�����ȷ����
A��COS�����У�����ԭ�Ӷ�����8���ӵ��ȶ��ṹ
B��COS�����Ǻ��м��Լ��ķǼ��Է���
C��COS����������ԭ�Ӵ���ͬһֱ����
D��COS������O2��ȼ��
���ʻ���COS��������������Һ���������õĹ�������ͼ��
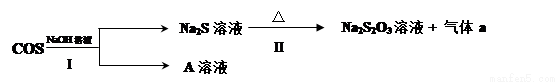
��֪A��һ���Σ���A�Ļ�ѧʽΪ �����嵥��aΪ ��
��3���ں����ܱ������У�CO��H2S��ϼ��������ʻ���ķ�ӦΪCO(g)+H2S(g) COS(g)+H2(g)����ӦǰCO��H2S�����ʵ�����Ϊ10 mol��ƽ���CO�����ʵ���Ϊ8 mol���ش��������⣺
COS(g)+H2(g)����ӦǰCO��H2S�����ʵ�����Ϊ10 mol��ƽ���CO�����ʵ���Ϊ8 mol���ش��������⣺
�������¶ȣ�H2SŨ�����ӣ������÷�Ӧ��___________________��Ӧ������ȡ������ȡ�����
��ƽ��ʱ������ͨ��CO 10 mol��H2S 10 mol��һ��ʱ����ٴδﵽƽ�⣬��ʱH2S��ת����______���������С���������䡰����
��4������Ӧ�ں����ܱ������н��У���˵���÷�Ӧ�Ѵﵽƽ��״̬����
a�������������ܶȱ��ֲ���
b��CO��H2S��COS��H2��Ũ�Ⱦ����ٱ仯
c��c(H2)��c(H2S��
d����(H2)������(H2S)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������һ�и�һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���ſ�ѧ�����IJ��Ͻ������о����ʵ��ֶκ�;��Խ��Խ�࣬N5+��H3��O4��C60���ѱ����֡������й�˵���У���ȷ����
A. N5+�������36������
B. O2��O4����ͬλ��
C. C60�Ƚ��ʯ�۵��
D. H2��H3����ͬ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ�����и�һ��ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ȥ���и��������е��������ʣ������Լ��ͷ�������ȷ����
| ���� | ���� | �������õ��Լ��ͷ��� |
A | CaO���� | CaCO3���� | ����������ϡ���� |
B | NaOH��Һ | Ca(OH)2��Һ | ��Һ��ͨ��CO2���ٹ��� |
C | CO2���� | CO���� | ��ȼ |
D | ͭ�� | ���� | �ȼ����������ᣬ�ٹ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���ຣʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ������
A��B��C��D��EΪԭ��������������Ķ�����Ԫ�أ���֪A��B��E 3��ԭ������㹲��11�����ӣ�����3��Ԫ�ص�����������ˮ�����������ܷ�����Ӧ�����κ�ˮ��CԪ�ص������������ȴ�����������4��DԪ��ԭ�Ӵ�����������������������3��
��1��д������Ԫ�ط��ţ�
A ��B ��C ��D ��E
��2��A��E��Ԫ�ؿ��γɻ�����õ���ʽ��ʾ�仯������γɹ��̣� ��
��3��д��A��B��Ԫ�ص�����������ˮ�������Ӧ�Ļ�ѧ����ʽ�� ��
��4��д��B��E��Ԫ�ص�����������ˮ�������Ӧ�����ӷ���ʽ�� ��
��5��C��D��E���⻯���ȶ�����ǿ��������Ϊ�����û�ѧʽ��ʾ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���ຣʡ��һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
������̬�⻯������ȶ����� �� ��
A. HF B. HI C. HBr D. HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��������������ѧԺ���и�һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���Ϊ1L��ij��Һ���ܺ���Cl-��NO3-��SO42-��CO32-��NH4+��Fe2+��Al3+��Ba2+��K+��ȡ����Һ100ml���������NaOH��Һ�����ȣ��õ�0.02mol���壬ͬʱ�����İ�ɫ����Ѹ�ٱ�Ϊ����ɫ�����ˡ�ϴ�ӡ����գ��õ�1.6g���壻��������Һ�м�������BaCl2��Һ���õ�4.66g����������ij���������������ȷ����
A����Һ�е���Ҫ���ӽ�ΪSO42-��Fe2+��NH4+
B��Cl��һ�����ڣ���c��Cl����=0.2mol��L-1
C����ԭ��Һ�м������ᣬ��������������
D��CO32-��Al3+һ�������ڣ�K+���ܴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ�߶�����ĩ��ѧ�Ծ��������棩 ���ͣ�ʵ����
�����������γɵĸ�����ʯ��(CaSO4��2H2O��ת��Ϊ����ط��Ϻ��Ȼ���ˮ���ﴢ�Ȳ��ϣ����۴Ӿ���Ч�桢��Դ�ۺ����û��Ǵӻ��������Ƕȿ���������Ҫ���塣������ʯ��ת��Ϊ����غ��Ȼ��ƵĹ�������ʾ��ͼ��
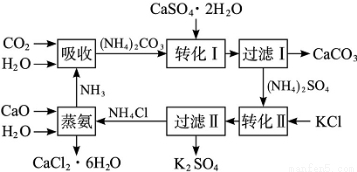
��1�������������õ�ԭ�ϳ�CaSO4��2H2O�⣬����Ҫ____________��ԭ�ϡ�
��2��д��ʯ������Һ�м���̼�����Һ������Ӧ�����ӷ���ʽ��__________________��
��3�����ˢ����������Һ��(NH4��2SO4��Һ��������Һ�к���CO32���ķ����ǣ�_______________��
��4���Ȼ��ƽᾧˮ����(CaCl2��6H2O����Ŀǰ���õ������Ȳ��ϣ�ѡ���������________��
a���۵�ϵ�(29 ���ۻ��� b���ܵ��� c��������ˮ d����
��5����������������������ɫ��ѧ�������_________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com