
【题目】已知热化学方程式:
SO2(g)+1/2O2(g)![]() SO3(g)ΔH=-98.32 kJ/mol,在容器中充入2 mol SO2和1 mol O2充分反应,最终放出的热量为
SO3(g)ΔH=-98.32 kJ/mol,在容器中充入2 mol SO2和1 mol O2充分反应,最终放出的热量为
A. 196.64 kJ B. 196.64 kJ/mol C. <196.64 kJ D. >196.64 kJ
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是:
A.原子晶体的熔点一定高于离子晶体
B.P4 和 CH4 都是正四面体分子,键角都为 109°28’
C.NaCl 晶体中与每个 Na+距离相等且最近的 Na+共有 6 个
D.C60 气化和 I2 升华克服的作用力相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉钼矿的主要成分是MoS2(Mo呈+4价),含少量SiO2以及Re的化合物等杂质。由辉钼矿可制得金属缓蚀剂钼酸钠晶体(Na2MoO4·10H2O)、催化剂Mo2C和氧化剂KReO4,其主要流程如下:

(1)焙烧辉钼矿时发生的反应及反应开始的温度(T)与真空度的关系如下图所示:(真空度P/P0表示反应时的压强与标准大气压之比)

为获得碳化钼,在真空度为0.5的条件下,适宜的反应温度应控制___________。
(2)焙烧时,生成Mo2C的反应中被还原的元素有___________(填元素符号);水洗烧结物时,洗去的物质除Na2S、Na2CO3之外,还有___________。
(3)用 NaClO2氧化MoS2时,MoS2转化为MoO42-和SO42-,写出该反应的离子方程式___________。
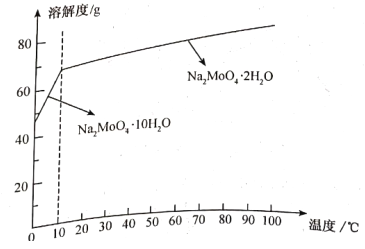
(4)已知钼酸钠的溶解度曲线如下图,获得Na2MoO4·10H2O的操作A为___________、___________、过滤。
(5)生成KReO4晶体的化学方程式为___________;加入KCl时,同时加入乙醇的作用是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,浓度都是1mol·L-1的两种气体X2和Y2在密闭容器中反应,经过tmin后,测得物质的浓度分别为:c(X2)=0.4mol·L-1,c(Y2)=0.8mol·L-1,则该反应的方程式可表示为()
A. X2+2Y2![]() 2XY2B. 2X2+Y2
2XY2B. 2X2+Y2![]() 2X2Y
2X2Y
C. X2+3Y2![]() 2XY3D. 3X2+Y2
2XY3D. 3X2+Y2![]() 2X3Y
2X3Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理(平衡移动原理)解释的是
①铁在潮湿的空气中容易生锈
②二氧化氮与四氧化氮的平衡体系,加压缩小体积后颜色加深
③实验室可用排饱和食盐水的方法收集氯气
④钠与氯化钾共融制备钾 Na(l)+KCl(l)![]() K(g)+NaCl(l)
K(g)+NaCl(l)
⑤开启啤酒瓶后,瓶中马上泛起大量泡沫
A. ③④ B. ①② C. ①⑤ D. ①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,一定体积的密闭容器中有如下平衡:H2(g)+I2(g)![]() 2HI(g)。已知H2和I2的起始浓度均为0.10 mol·L-1时,达平衡时HI的浓度为0.16 mol·L-1。若H2和I2的起始浓度均变为0.20 mol·L-1,则平衡时H2的浓度(mol·L-1)是
2HI(g)。已知H2和I2的起始浓度均为0.10 mol·L-1时,达平衡时HI的浓度为0.16 mol·L-1。若H2和I2的起始浓度均变为0.20 mol·L-1,则平衡时H2的浓度(mol·L-1)是
A. 0.16 B. 0.08 C. 0.04 D. 0.02
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com