
【题目】粗盐提纯时,在溶解、过滤、蒸发各步实验中都用到的仪器是 .
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:
【题目】下列变化中,属于吸热反应的是( )
①液态水的汽化 ②将胆矾加热变为白色粉末
③浓硫酸稀释 ④KCl03分解制氧气
⑤生石灰跟水反应生成熟石灰
⑥CaCO3高温分解⑦CO2+C![]() 2CO
2CO
⑧Ba(OH)2·8H2O与固体NH4Cl混合
⑨C(s)+H2O(g)![]() CO(g)+H2(g)⑩Al与盐酸反应
CO(g)+H2(g)⑩Al与盐酸反应
A. ②③④⑤⑥⑦⑧⑨ B.②④⑥⑦⑧⑨ C.②④⑥⑧ D.②③④⑧⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知常温下E为无色无味的液体,F为淡黄色粉末,G为常见的无色气体(反应条件均已略去) ,请回答下列问题:
(1)请写出F的化学式 ;在②反应中,当生成2.24L的G(标准状况)时,反应中转移的电子的物质的量为 moL。
(2)若A、C、D均含有氯元素,且A中的化合价介于C与D之间,写出反应①的离子方程式: 。
(3)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B分别为 、 。(写化学式)
(4)若A与B均为固体化合物,D是一种能使湿润的红色石蕊试纸变蓝的气体,反应①是实验室制备D的反应,则反应①的化学方程式为 。
Ⅱ.A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应产物略去)。
![]()
(1)若A是一种黄色非金属单质固体,则B→C的化学方程式为 。
(2)若A是一种活泼金属,C是淡黄色固体,则C的电子式为 ,写出C和CO2反应的化学方程式,并标出单线桥 。
(3)若A是碱性气体,试写出A与氧气反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.按要求写出下列反应的热化学方程式:
(1)在25℃、101kPa下,1g甲醇液体燃烧生成C02和液态水时放热22.0kJ。则表示甲醇燃烧热的热化学方程式为__________________________。
(2)若适量的N2和02完全反应,每生成23g N02需要吸收16.0kJ热量,此反应的热化学方程式为___________________。
Ⅱ.对于下列三个反应,从正反开始进行达到平衡后,保持温度、体积不变,按要求回答下列问题:
(1)PCl5(g)![]() PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
再充入PCl5(g),平衡向___________方向移动(填“正反应”或“逆反应”),达到平衡后,PCl5(g)的转化率___________(填“增大”、“减小”或“不变”,下同)。
(2)2HI(g)![]() I2(g)+H2(g)
I2(g)+H2(g)
再充入HI(g),平衡向___________方向移动,达到平衡后,HI的分解率___________。
(3)2NO2(g)![]() N2O4(g)
N2O4(g)
再充入N2O4(g),平衡向___________方向移动,达到平衡后,NO2(g)的转化率___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在体积为2L的密闭容器中,气态物质A、B、C的物质的量n(mo1)随时间t的变化如图2-10-2所示。已知达平衡后,降低温度,A的转化率将增大。
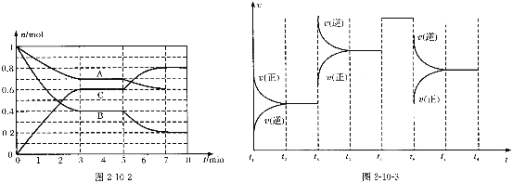
(1)根据图2-10-2数据,写出该反应的化学方程式________________;此反应的平衡常数表达式K=______________。从反应开始到达第一次平衡时的平均反应速率v(A)为_________。
(2)在5~7min内,若K值不变,则此处曲线变化的原因是________________。
(3)图2-10-3表示此反应的反应速率v和时间t的关系。各阶段的平衡常数如下表所示:
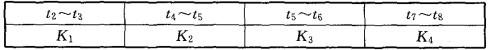
根据图2-10-3判断,在t3和t6时刻改变的外界条件分别是__________和____________;K1、K2、K3、K4之间的关系为__________(用“>”“<”或“=”连接)。平衡时A的转化率最大的一段时间是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的密闭容器中发生可逆反应:mA(g)+nB(g)![]() pC(g)+qD(g),当m、n、p、q为任意整数(不为零)时,一定能说明达到平衡状态的标志是( )
pC(g)+qD(g),当m、n、p、q为任意整数(不为零)时,一定能说明达到平衡状态的标志是( )
A. 各组分的浓度不再改变
B. 体系的压强不再改变
C. 反应速率vA:vB:vC:vD=m:n:p:q
D. 单位时间内m mol A断键发生反应,同时n mol B也断键发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com