
【题目】下列说法中正确的是
A.用完的电池可以随意丢弃
B.增加炼铁高炉的高度可以降低尾气中CO的含量
C.无论加入正催化剂还是加入负催化剂都能大大提高化学反应速率
D.把煤粉碎了再燃烧可以提高煤的燃烧效率
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.不需要加热就能发生的反应是放热反应
B.构成原电池正极和负极的材料必须是两种金属
C.化学能是能量的一种形式,它不仅可以转化为热能,也能转化为电能
D.马口铁(镀锡铁)破损时与电解质溶液接触,锡先被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示。则下列说法中正确的是
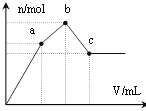
A. a点的溶液呈中性
B. 从开始到b点发生反应的总的离子方程式是:Al3++2SO42-+2Ba2++3OH-= Al(OH)3↓+2BaSO4↓
C. c点加入Ba(OH)2溶液的体积为200 mL
D. c点溶液呈碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H3BO3(一元弱酸) 可以通过电解NaB(OH)4溶液的方法制备,其工作原理如图,下列叙述错误的是

A. M室发生的电极反应式为:2H2O-4e- = O2↑+4H+
B. N室中:a% <b%
C. 理论上每生成1mol产品,阴极室可生成标准状况下5.6L气体
D. b膜为阴膜,产品室发生反应的化学原理为强酸制弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为2L的恒容密闭容器中发生反应xA (g) +yB (g) ![]() zC (g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n (A): n (B)的变化关系则下列结论正确的是
zC (g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n (A): n (B)的变化关系则下列结论正确的是
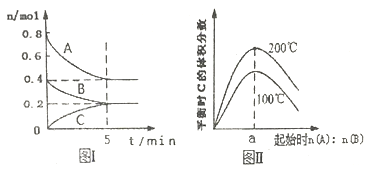
A. 200℃时,反应从开始到平衡的平均速率v(B)=0.04 molL-1min-1
B. 图Ⅱ所知反应xA(g)+yB(g)![]() zC(g)的ΔH<0,且a=2
zC(g)的ΔH<0,且a=2
C. 若在图Ⅰ所示的平衡状态下,再向体系中充入He,重新达到平衡前v正>v逆
D. 200℃时,向容器中充入2 mol A 和1 mol B,达到平衡时,A 的体积分数小于50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室进行氨气快速制备与性质实验的组合装置,部分固定装置未画出. 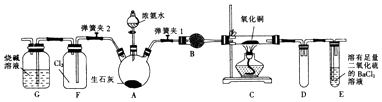
(1)在组装好装置之后,应进行的操作名称是 .
(2)装置B中盛放的试剂是 .
(3)当C中固体全部变为红色后,关闭弹簧夹1,慢慢移开酒精灯,待冷却后,称量C中固体质量,若反应前固体质量为16g,反应后固体质量减少2.4g,则该固体产物的成分是(用化学式表示).从E中逸出液面的气体可以直接排入空气中,请写出在C中发生反应的化学方程式: .
(4)关闭弹簧夹1,打开弹簧夹2,气体进入F中立即产生白烟,同时发现G中溶液迅速倒吸流入F中.请写出产生白烟的化学方程式: , 迅速发生倒吸的原因是 .
(5)为了证明一水合氨是弱碱,甲、乙两同学分别设计如下实验进行探究. ①甲同学用pH试纸测得室温下0.01molL﹣1氨水的pH为10,则认定一水合氨是弱电解质,理由是 .
②乙同学取出10mL 0.1molL﹣1氨水,滴入2滴酚酞试液,溶液显粉红色,再加入少量NH4Cl晶体,观察到 , 证明一水合氨是弱电解质.
③请设计一个与甲、乙同学不同的简单实验方案,证明一水合氨是弱电解质: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用图示装置进行下列实验,能达到实验目的的是
溶液a | 固体b | 溶液c | 实验目的:验证 |
| |
A | 浓硝酸 | NaHCO3 | Na2SiO3 | 非金属性:N>C>Si | |
B | 浓盐酸 | KMnO4 | Na2S | 氧化性:KMnO4>Cl2>S | |
C | 浓盐酸 | CaCO3 | NaAlO2 | 酸性:HCl>H2CO3>Al(OH)3 | |
D | 浓氨水 | CaO | 酚酞溶液 | NH3·H2O是弱碱 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀溶液中含有4 mol KNO3和2.5 mol H2SO4,向其中加入1.5 mol Fe,充分反应(已知NO![]() 被还原为NO),最终溶液体积为1L。下列说法正确的是( )
被还原为NO),最终溶液体积为1L。下列说法正确的是( )
A. 反应后生成NO的体积为33.6 L (标况)
B. 所得溶液中c(Fe2+)∶c(Fe3+)=1∶2
C. 所得溶液中c(NO![]() )=2.75 mol·L-1
)=2.75 mol·L-1
D. 所得溶液中的溶质只有FeSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。
![]()
下列说法中不正确的是( )
A. 当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B. 当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C. B和Cl2的反应是氧化还原反应
D. 当X是强酸时,C在常温下是气态单质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com