


科目:高中化学 来源: 题型:
| A、Br2+2HI═I2+2HBr |
| B、2FeCl2+Cl2═2FeCl3 |
| C、2FeCl2+2HCl+I2═2FeCl3+2HI |
| D、Cl2通入到NaBr和NaI的混合溶液中:I-先被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钠的摩尔质量是40 g |
| B、1 mol H2O中含有2 mol氢和1 mol氧 |
| C、0.012 kg12C中含有约6.02×1023个碳原子 |
| D、2 mol水的摩尔质量是1 mol水的摩尔质量的2倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由碳、氢、氮三种元素组成 |
| B、所有N、C原子都在同一平面上 |
| C、分子中所有的N原子均是sp3杂化 |
| D、分子式为C2H8N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 0.2mol某一元醇,在密闭容器中燃烧后,其产物为CO2、CO、H2O.产物通过浓H2SO4后,浓H2SO4增重10.8g;再通过灼热的CuO充分反应后,CuO失重3.2g;最后通过碱石灰,碱石灰增重17.6g.
0.2mol某一元醇,在密闭容器中燃烧后,其产物为CO2、CO、H2O.产物通过浓H2SO4后,浓H2SO4增重10.8g;再通过灼热的CuO充分反应后,CuO失重3.2g;最后通过碱石灰,碱石灰增重17.6g.查看答案和解析>>
科目:高中化学 来源: 题型:
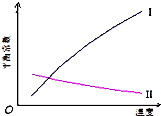 醇脱水反应在不同温度条件下得到的产物组成不同.下表是常压、某催化剂存在条件下,分别以等量乙醇在不同温度下进行脱水实验获得的数据,每次实验反应时间均相同.
醇脱水反应在不同温度条件下得到的产物组成不同.下表是常压、某催化剂存在条件下,分别以等量乙醇在不同温度下进行脱水实验获得的数据,每次实验反应时间均相同.| 温度(℃) | 乙醇转化率(%) | 有机产物含量(体积分数) | |
| 乙烯(%) | 乙醚(%) | ||
| 125 | 20 | 8.7 | 90.2 |
| 150 | 68 | 16.7 | 82.2 |
| 175 | 88 | 32.3 | 66.8 |
| 200 | 90 | 86.9 | 12.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 工业上可采用电化学法利用H2S废气制取氢气,该法制氢过程的示意图如图所示,回答下列问题:
工业上可采用电化学法利用H2S废气制取氢气,该法制氢过程的示意图如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氮的氧化物是光化学烟雾的主要污染物,二氧化碳是温室效应的主要污染物,所以他们的含量是空气质量报告的主要项目 |
| B、严格讲,“通风橱”是一种不负责任的防污染手段,因为实验产生的有害气体没有得到转化或吸收 |
| C、开发利用新能源,合理利用工业生产的废热,是缓解能源危机的重要途径 |
| D、用二氧化硫、亚硝酸钠、苏丹红等化学药品“美化”后的食物“味美、色艳”,但添加剂超标,对人体危害极大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com