
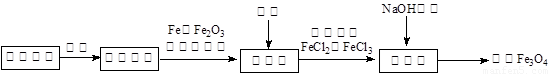
活性Fe3O4为黑色固体,有磁性,其不溶于水、碱和酒精、乙醚等有机溶剂中, Fe3O4在潮湿的空气中或高温下易被O2氧化。工业上利用锈蚀废铁为原料,利用共沉淀法制备活性Fe3O4(或写为FeO·Fe2O3)的流程如下:
(1)在制备过程中将块状固体原料粉碎磨成粉末,作用是 。
(2)设计合理的实验方案证明Fe3O4与盐酸反应的产物中含有Fe2+、Fe3+,简述实验操作步骤和实验现象 。
(可供选择的试剂:KSCN溶液、还原铁粉、氯水、酸性高锰酸钾溶液)
(3)假如在反应池中几乎没有气体产生,在合成池里所有铁元素转化为Fe3O4,则根据相关反应可知,配料中心很可能使混合物中的Fe2O3与Fe物质的量之比接近于 。
(4)在一次制备Fe3O4的实验中,由于配料中心反应物比例控制不当,获得了另一种产品FexOy。取一定量该产品溶于足量盐酸中,还需通入标准状况下224 mLCl2才能把溶液中的Fe2+全部氧化为Fe3+,然后把所得溶液滴加足量NaOH溶液,将沉淀过滤、洗涤、蒸干,灼烧至恒重,得8 g固体。计算该产品的化学式。(请写出计算过程)
(1)有利于加快反应池中反应速率
(2)取2份待检液,其中一份待检液滴入KSCN溶液,若显示血红色则含有Fe3+,再向另一份待检液滴入酸性高锰酸钾溶液,若紫红色褪去则含有Fe3+
(3)4:1(3分) (4) Fe5O7或FeO·2Fe2O3(5分)除标示外,其余每空2分
【解析】
试题分析:(1)在制备过程中将块状固体原料粉碎磨成粉末,作用是增大反应物的接触面积,有利于加快反应池中反应速率 。(2)由于Fe3O4不溶于水但能溶于酸,如与盐酸反应的产物中含有Fe2+、Fe3+,可分别对两种离子进行检验,根据提供的试剂方法如下:取2份待检液,其中一份待检液滴入KSCN溶液,若显示血红色则含有Fe3+,再向另一份待检液滴入酸性高锰酸钾溶液,若紫红色褪去则含有Fe3+。(3)没有气体产生,说明铁刚好使三价铁转化为二价铁,由于在1molFe3O4中可以认为有二价的氧化亚铁和三价的三氧化铁各1mol,设Fe为Xmol,Fe2O3为ymol,生成1molFe3O4,根据Fe+2Fe3+=3Fe2+则有:X+2Y=3,3X=1,解得X=1/3;Y=4/3,故铁和三氧化铁的物质的量为1:4。(4)在一次制备Fe3O4的实验中,由于配料中心反应物比例控制不当,获得了另一种产品FexOy。取一定量该产品溶于足量盐酸中,还需通入标准状况下224 mLCl2才能把溶液中的Fe2+全部氧化为Fe3+,然后把所得溶液滴加足量NaOH溶液,将沉淀过滤、洗涤、蒸干,灼烧至恒重,得8 g固体。计算该产品的化学式。(请写出计算过程) 根据2Fe2++Cl2=2Fe3+ +2 Cl-,由224 mLCl2可知氯气的物质的量为0.01mol,Fe2+为0.02mol。得到8 g固体为三氧化二铁,物质的量为0.05mol,则Fe3+为0.03mol,故化学式为Fe10O13或4FeO·3Fe2O3。
考点:本考点属于物质的推断题,做本类题型时,要注意题目给出的信息,利用已知条件来解决有关的问题.考查了金属铁的化学性质,和相关计算。


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com